题目内容
第三周期中置换H能力最强的是 元素(符号),化学性质最稳定的元素符号是 ,最高价氧化物对应的水化物酸性最强的分子式为 ,碱性最强的分子式为 ,显两性的分子式为 ,原子半径最大的金属元素的符号是 ,离子半径最小的金属离子结构示意图 .
分析:同周期元素从左到右元素的金属性逐渐减弱,非金属性逐渐增强,以此判断对应的单质、化合物的相关性质.
解答:解:同周期元素从左到右元素的金属性逐渐减弱,非金属性逐渐增强,
则置换酸中氢的能力最强的元素为金属性最强的元素为Na;碱性最强的化合物为NaOH;
化学性质最稳定的元素为0族元素,第三周期元素为Ar;
最高价氧化物的水化物的酸性最强的化合物对应的元素为Cl元素,对应的酸为HClO4;
第三周期中的两性氢氧化物为Al(OH)3;
同周期元素从左到右元素原子半径逐渐减小,则原子半径最大的是Na;
离子半径最小的离子为Al3+,离子结构示意图是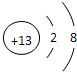 .
.
故答案为:Na;Ar;HClO4;NaOH;Al(OH)3;Na;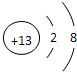 .
.
则置换酸中氢的能力最强的元素为金属性最强的元素为Na;碱性最强的化合物为NaOH;
化学性质最稳定的元素为0族元素,第三周期元素为Ar;
最高价氧化物的水化物的酸性最强的化合物对应的元素为Cl元素,对应的酸为HClO4;
第三周期中的两性氢氧化物为Al(OH)3;
同周期元素从左到右元素原子半径逐渐减小,则原子半径最大的是Na;
离子半径最小的离子为Al3+,离子结构示意图是
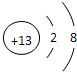 .
.故答案为:Na;Ar;HClO4;NaOH;Al(OH)3;Na;
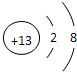 .
.点评:本题考查同周期元素性质的递变规律,题目难度不大,注意加强对基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目