题目内容
1.某含(NH4)2SO4和K2SO4的混合溶液100mL,向其中滴加足量的Ba(OH)2溶液,加热,充分反应,生成的气体在标准状况下体积为448mL,将反应后的溶液过滤得白色沉淀4.66g.求原混合溶液中K2SO4的物质的量浓度.分析 滴加足量的Ba(OH)2溶液,加热,充分反应生成的气体在标准状况下体积为448mL,该气体为氨气;将反应后的溶液过滤得白色沉淀4.66g,该沉淀为硫酸钡,根据n=$\frac{m}{M}$计算出硫酸钡的物质的量,根据$\frac{V}{{V}_{m}}$计算出氨气的物质的量,先利用N原子守恒计算出硫酸铵的物质的量,再利用硫酸根离子守恒计算出硫酸钾的物质的量,最后根据c=$\frac{n}{V}$计算出硫酸钾的物质的量浓度.
解答 解:生成的4.66g沉淀为硫酸钡,硫酸钡的物质的量为:$\frac{4.66g}{233g/mol}$=0.02mol,
生成的气体为氨气,标准状况下448mL氨气的物质的量为:$\frac{0.448L}{22.4L/mol}$=0.02mol,根据N原子守恒可知混合液中(NH4)2SO4的物质的量为:0.02mol×$\frac{1}{2}$=0.01mol,
则混合液中K2SO4的物质的量为:0.02mol-0.01mol=0.01mol,
所以混合液中硫酸钾的物质的量浓度为:$\frac{0.01mol}{0.1L}$=0.1mol/L,
答:原混合溶液中K2SO4的物质的量浓度为0.1mol/L.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确物质的量与物质的量浓度、摩尔质量、气体摩尔体积之间的关系为解答关键,试题培养了学生的化学计算能力.

练习册系列答案
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
11.某学生鉴定甲盐溶液的流程如图所示,下列说法正确的是( )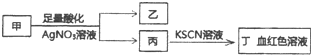

| A. | 若乙为白色沉淀,则甲可能含有SiO32- | |
| B. | 若乙为黄色沉淀,则甲可能为FeI3 | |
| C. | 若乙为浅黄色沉淀,则甲可能含有S2- | |
| D. | 若乙为浅黄色沉淀,则甲可能是FeBr2 |
12.下列过程中属于人工固氮的是( )
| A. | 雷雨天气时产生少量NO | |
| B. | 往农田中施放铵态氮肥 | |
| C. | 豆科植物等根部的根瘤菌吸收空气中的氮气转变为氨 | |
| D. | N2和H2在高温、高压和催化剂存在下合成氨 |
16.除去下列物质中的杂质(括号中为杂质),所用试剂和方法错误的是( )
| A. | Cu (CuO),加盐酸,过滤 | B. | NaCl (I2)固体,加热升华 | ||
| C. | KNO3 (K2SO4),加BaCl2溶液,过滤 | D. | MgO (Al2O3),加烧碱溶液,过滤 |
13.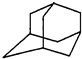 如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )
如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )
 如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )
如图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂.下列有关说法中正确的是( )| A. | 金刚烷的分子中有18个碳原子 | |
| B. | 1-溴金刚烷的结构有2种 | |
| C. | 金刚烷属于烷烃的同系物 | |
| D. | 金刚烷应该具有和芳香烃相似的化学性质 |
11.下列反应是氧化还原反应的是( )
| A. | NaOH+HCl═NaCl+H2O | B. | CuO+H2SO4═CuSO4+H2O | ||
| C. | Zn+2H+═Zn2++H2↑ | D. | CaO+H2O═Ca(OH)2 |
