题目内容
原子结构决定元素的性质,下列说法中,正确的是( )
| A、Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小 |
| B、在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的其沸点也一定最高 |
| C、第2周期元素的最高正化合价都等于其原子的最外层电子数 |
| D、非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:A.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
B.ⅥA族中O元素非金属性最强,氢化物最稳定,水分子中存在氢键,沸点最高;
C.O元素、F元素没有最高正化合价;
D.元素非金属性越强,其最高价氧化物对应水化物的酸性越强.
B.ⅥA族中O元素非金属性最强,氢化物最稳定,水分子中存在氢键,沸点最高;
C.O元素、F元素没有最高正化合价;
D.元素非金属性越强,其最高价氧化物对应水化物的酸性越强.
解答:
解:A.Na+、Al3+电子层结构相同,Al的核电荷数大,离子半径较小,Cl-的电子层最多,离子半径最大,故A错误;
B.ⅥA族中O元素非金属性最强,氢化物最稳定,而水分子中存在氢键,其沸点最高,故B正确;
C.O元素、F元素没有最高正化合价,故C错误;
D.元素非金属性越强,其最高价氧化物对应水化物的酸性越强,不是最高价含氧酸,氧化物对应水化物的酸性不一定,如非金属性Cl>S,次氯酸是弱酸、硫酸是强酸,故D错误,
故选B.
B.ⅥA族中O元素非金属性最强,氢化物最稳定,而水分子中存在氢键,其沸点最高,故B正确;
C.O元素、F元素没有最高正化合价,故C错误;
D.元素非金属性越强,其最高价氧化物对应水化物的酸性越强,不是最高价含氧酸,氧化物对应水化物的酸性不一定,如非金属性Cl>S,次氯酸是弱酸、硫酸是强酸,故D错误,
故选B.
点评:本题考查结构与性质关系,需要学生熟练掌握基础知识,注意氢键对物质性质的影响、化合价特殊性.

练习册系列答案
相关题目
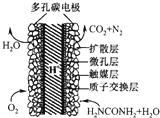 电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )
电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )| A、电池工作时H+移向负极 |
| B、该装置还可以将电能转化成为化学能 |
| C、电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+ |
| D、理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1mol/L KMnO4溶液:K+、Na+、I-、Cl- |
| B、能溶解Al2O3的溶液:Na+、K+、HCO3-、NO3- |
| C、加入KSCN显红色的溶液:K+、Mg2+、Cl-、SO42- |
| D、水电离出c(OH-)=10-5mol/L的溶液:Na+、Fe2+、Cl-、NO3- |
下列各项中,两种物质间反应均产生1mol气体时,参加反应的酸的物质的量最少的是( )
| A、碳与浓硝酸 |
| B、铜与浓硫酸 |
| C、锌与稀硫酸 |
| D、二氧化锰与浓盐酸 |
设NA为阿伏加德罗常数,下列说法中不正确的是( )
| A、2.3g金属钠变为钠离子时失去的电子数是0.1NA |
| B、标准状况下,11.2L四氯化碳所含分子数为0.5NA |
| C、32g氧气所含原子数为2NA |
| D、18g水所含的质子总数为10 NA |
以下反应最符合绿色化学,原子经济性要求的是( )
| A、乙烯聚合为聚乙烯高分子材料 |
| B、甲烷与氯气制备一氯甲烷 |
| C、以铜和浓硝酸为原料生产硝酸铜 |
| D、乙醇催化氧化制乙醛 |
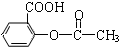 ).为测定某解热镇痛药阿斯
).为测定某解热镇痛药阿斯 冷却后用0.10mol/L HCl溶液返滴过量的NaOH,消耗该HCl溶液25.00mL.
冷却后用0.10mol/L HCl溶液返滴过量的NaOH,消耗该HCl溶液25.00mL.