题目内容
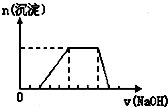 某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:从图中沉淀量随之氢氧化钠的加入量增加变化情况结合离子的性质可知:开始发生酸碱中和,然后Al3+与碱反应,再NH4+与碱反应,最后沉淀与碱反应完全溶解,依据各段发生反应消耗的氢氧化钠的物质的量计算各种离子的物质的量.
解答:
解:由图可知,开始发生酸碱中和,然后Al3+与碱反应,再NH4+与碱反应,最后沉淀与碱反应完全溶解,所以溶液中含有的离子有:H+,Al3+,NH4+,一定不含的离子为:Mg2+,Fe3+,过程中依次发生的反应为:H++OH-=H2O;Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=[Al(OH)4]-;则有图消耗氢氧化钠的物质的量可知:
H++OH-=H2O; Al3++3OH-=Al(OH)3↓; NH4++OH-=NH3?H2O;
1 1 1 3 1 1
n(H+) 2mol n(Al3+) 3mol n(NH4+)3mol
所以n(H+)=2mol; n(Al3+)=1mol;n(NH4+)=3mol;
n(H+):n(Al3+):n(NH4+)=2:1:3;最后沉淀与碱反应完全溶解,而氢氧化镁、氢氧化铁在氢氧化钠中不溶解,故一定不含:Mg2+,Fe3+;
故答案为:H+,Al3+,NH4+;1:2:3;Mg2+,Fe3+.
H++OH-=H2O; Al3++3OH-=Al(OH)3↓; NH4++OH-=NH3?H2O;
1 1 1 3 1 1
n(H+) 2mol n(Al3+) 3mol n(NH4+)3mol
所以n(H+)=2mol; n(Al3+)=1mol;n(NH4+)=3mol;
n(H+):n(Al3+):n(NH4+)=2:1:3;最后沉淀与碱反应完全溶解,而氢氧化镁、氢氧化铁在氢氧化钠中不溶解,故一定不含:Mg2+,Fe3+;
故答案为:H+,Al3+,NH4+;1:2:3;Mg2+,Fe3+.
点评:本题考查了离子的鉴别,题目难度不大,熟悉相关离子的性质、明确图象中各段的含义及发生的反应是解题关键,注意铝离子的性质.

练习册系列答案
相关题目
双羟基铝碳酸钠[NaAl(OH)2CO3]是医疗上常用的一种抑酸剂,与奥美拉唑、胃舒平等药物具有同等药效.关于该物质的说法正确的是( )
| A、该物质属于两性氢氧化物 |
| B、该物质是Al(OH)3和Na2CO3的混合物 |
| C、1 mol NaAl(OH)2CO3最多可消耗4 mol H+ |
| D、该药剂适合于胃溃疡患者服用 |
废旧电池集中处理的首要原因是( )
| A、回收电池中的石墨电极 |
| B、回收电池外壳的金属材料 |
| C、防止电池中汞、镉等重金属对土壤和水源的污染 |
| D、防止电池中的渗出液腐蚀其他物品 |