题目内容
3.现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).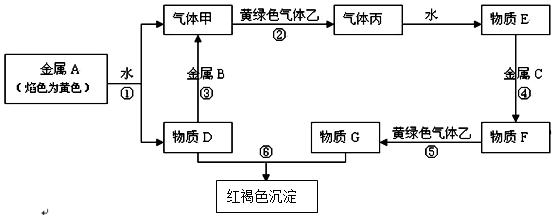
请根据以上信息回答下列问题:
(1)写出金属元素A的原子结构示意图:
 .
.(2)写出下列反应的离子方程式:反应③2Al+2OH-+2H2O=2AlO2-+3H2↑;反应⑤2Fe2++Cl2═2Fe3++2Cl-
(3)检验物质G中阳离子的操作方法取物质G少许于试管中,向其中滴加少量的KSCN溶液,溶液变为血红色(或红色),证明物质G中有Fe3+离子.
(4)实验室制取黄绿色气体乙的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,在该反应中如有0.5mol乙生成,转移的电子的物质的量是1mol.制取完毕,多余的乙将用D的水溶液来吸收,其离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
分析 金属A焰色反应为黄色,故A为金属Na,由反应①可知,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,故金属B为Al.黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸.氢氧化钠与物质G反应生成红褐色沉淀是Fe(OH)3,故物质G中含有Fe3+,由转化关系HCl$\stackrel{金属C}{→}$物质F$\stackrel{Cl_{2}}{→}$物质G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3,结合物质的性质解答该题.
解答 解:(1)由以上分析可知,A为Na,原子结构示意图为 故答案为:
故答案为: ;
;
(2)反应③为铝与氢氧化钠反应生成偏铝酸钠和氢气,反应离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
反应⑤氯化亚铁与氯气反应生成氯化铁,反应离子方程式为:2Fe2++Cl2═2Fe3++2Cl-;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;2Fe2++Cl2═2Fe3++2Cl-;
(3)由以上分析可知,G为FeCl3,则物质G中阳离子的操作方法为取物质G少许于试管中,向其中滴加少量的KSCN溶液,溶液变为血红色(或红色),证明物质G中有Fe3+离子,
故答案为:取物质G少许于试管中,向其中滴加少量的KSCN溶液,溶液变为血红色(或红色),证明物质G中有Fe3+离子;
(4)黄绿色气体乙为Cl2,则实验室制取黄绿色气体乙的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,在该反应中如有0.5molCl2生成,转移的电子的物质的量是1mol,制取完毕,多余的Cl2将用NaOH的水溶液来吸收,其离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;1;Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题是考查物质推断与性质、常用化学用语,难度中等,掌握元素化合物的性质是解题的关键,需要学生熟练掌握元素化合物知识,注意特殊的颜色与特殊反应是推断的突破口.

| A. | 不能使酸性高锰酸钾溶液褪色 | |
| B. | 所有原子都在同一平面上 | |
| C. | 能使溴水褪色 | |
| D. | 与HCl在一定条件下能加成只得到一种产物 |
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
| A. | ${\;}_{a+m}^{b+m+n}R$ | B. | ${\;}_{a+m}^{b+a-m}R$ | C. | ${\;}_{a}^{b+a}R$ | D. | ${\;}_{a-m}^{a-m+b}R$ |
(I)经查:①Ksp(AgNO2)=2.0×10-8,Ksp(AgCl)=1.8×10-10;③Ka(HNO2)=5.1×10-4.请设计最简单的方法鉴别NaNO2和NaCl两种固体分别取两种固体样品少量于试管中加水溶解,再分别滴加酚酞试液,变红色的为NaNO2.
(Ⅱ)某化学实验小组用如图装置(略去夹持仪器)制备亚硝酸钠,并测定其产品的质量分数.
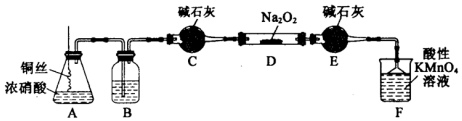
已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO和NO2均能与MnO4-反应生成NO3-和Mn2+.
(1)这样使用铜丝的优点是可以控制反应的发生与停止.
(2)装置A中发生反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;装置B中盛放的药品是C(填序号).
①浓硫酸②NaOH溶液③水④四氯化碳
(3)该小组取5.000g制取的样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.100mol•L-1酸性KMnO4溶液进行滴定,实验所得数据如表:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMn04溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O.
③该样品中亚硝酸钠的质量分数为69.0%.
| A. | 5; 0.1 | B. | 5; 0.2 | C. | 3<x<5; 0.1 | D. | 3<x<5; 0.2 |
| A | B | C | D | |
| 实验 | 分离汽油和水 | 通过蒸馏乙醇的水溶 液获得无水乙醇 | 分离 CCl4 中的 I2 | 除去 CO2 气体中的 HCl 气体 |
| 装 置 或 仪 器 | 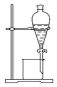 | 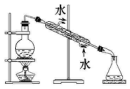 | 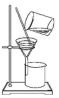 | 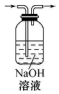 |
| A. | A | B. | B | C. | C | D. | D |
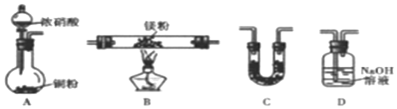
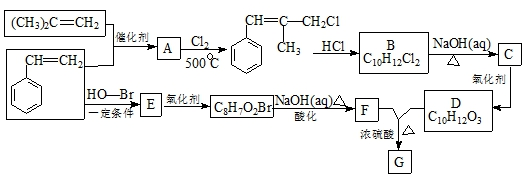
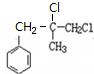 ,B生成C的反应类型为取代反应;
,B生成C的反应类型为取代反应;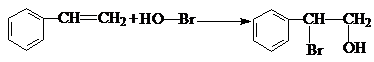 .
.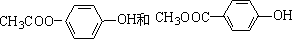 .
. ) 的合成线路:
) 的合成线路: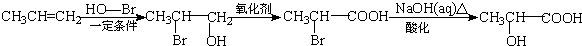 .
.