题目内容
下列说法不正确的是( )
| A、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| B、25℃与60℃时,0.005mol/L的硫酸溶液pH相等 |
| C、中和等体积、等物质的量浓度的盐酸和醋酸所消耗的n(NaOH)相等 |
| D、常温下,将pH=5的醋酸溶液稀释到原体积的1000倍后,溶液的pH≈7 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A.若NaHA溶液的pH<7,H2A也可能是弱酸;
B.强酸溶液中,强酸完全电离,溶液中氢离子浓度不随温度变化而变化;
C.中和醋酸和盐酸,消耗氢氧化钠的量与酸的物质的量成正比;
D.温度不变时,酸溶液无限稀释时不可能变为中性或碱性,只能接近中性.
B.强酸溶液中,强酸完全电离,溶液中氢离子浓度不随温度变化而变化;
C.中和醋酸和盐酸,消耗氢氧化钠的量与酸的物质的量成正比;
D.温度不变时,酸溶液无限稀释时不可能变为中性或碱性,只能接近中性.
解答:
解:A.若NaHA溶液的pH<7,H2A也可能是弱酸,如亚硫酸氢钠溶液呈酸性,但亚硫酸是弱酸,故A错误;
B.强酸溶液中,强酸完全电离,溶液中氢离子浓度不随温度变化而变化,所以25℃与60℃时,0.005mol/L的硫酸溶液中氢离子浓度相等,则pH相等,故B正确;
C.中和醋酸和盐酸,消耗氢氧化钠的量与酸的物质的量成正比,等体积等浓度的醋酸和盐酸的物质的量相等,所以消耗氢氧化钠的物质的量相等,故C正确;
D.温度不变时,酸溶液无限稀释时不可能变为中性或碱性,只能接近中性,所以常温下,将pH=5的醋酸溶液稀释到原体积的1000倍后,溶液的pH≈7,故D正确;
故选A.
B.强酸溶液中,强酸完全电离,溶液中氢离子浓度不随温度变化而变化,所以25℃与60℃时,0.005mol/L的硫酸溶液中氢离子浓度相等,则pH相等,故B正确;
C.中和醋酸和盐酸,消耗氢氧化钠的量与酸的物质的量成正比,等体积等浓度的醋酸和盐酸的物质的量相等,所以消耗氢氧化钠的物质的量相等,故C正确;
D.温度不变时,酸溶液无限稀释时不可能变为中性或碱性,只能接近中性,所以常温下,将pH=5的醋酸溶液稀释到原体积的1000倍后,溶液的pH≈7,故D正确;
故选A.
点评:本题考查了弱电解质的电离,涉及根据盐判断酸的强弱、弱电解质的电离等知识点,易错选项是CD,注意中和相同元数的酸时,消耗碱的物质的量与酸的物质的量成正比,与酸的强弱、浓度无关,D中酸或碱无限稀释时要考虑水的电离,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
汽车尾气(含有烃类、CO、NOx、SO2)是城市空气的主要污染源,治理方法之一是在汽车排气管上加装“催化转化器”,它使CO和NOx反应生成可参与大气生态环境循环的无毒气体,并使烃类充分燃烧及SO2转化,下列说法错误的是( )
| A、CO和NOx反应的化学方程式为:2xCO+2NOx=2xCO2+N2 |
| B、上述方法的缺点是由于CO2增多,会大大提高空气的酸度 |
| C、多植树造林,增大绿化面积,可有效控制城市空气各种污染源 |
| D、汽车改用天然气为燃料或开发氢能源,都会减少对空气的污染 |
已知某乳制品中富含钙元素,则下列食品中也富含钙元素的是( )
| A、水果 | B、动物肝脏 |
| C、海带 | D、豆类 |
下列物质分类正确的是( )
| A、SO2、CO2、CO均为酸性氧化物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、烧碱、纯醋酸、四氯化碳均为电解质 |
| D、空气、混凝土、氨水均为混合物 |
3molCl2和2molCO2相比较,下列叙述中正确的是( )
| A、分子数相等 | B、原子数相等 |
| C、体积相等 | D、质量相等 |
实验中的下列操作正确的是( )
| A、把试管中取量过多的Na2CO3溶液又倒入试剂瓶中 |
| B、将含有HNO3的废液倒入水槽中,再用水冲入下水道 |
| C、用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 |
| D、配制一定物质的量浓度的稀硫酸,浓硫酸溶于水后应冷却至室温才能转移到容量瓶中 |
图中有关电化学的示意图正确的是( )
A、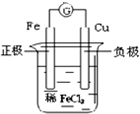 |
B、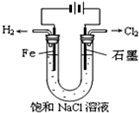 |
C、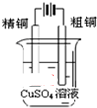 |
D、 |
 硼、碳、硅元素的单质及其化合物的构成自然界的重要物质.请回答下列问题:
硼、碳、硅元素的单质及其化合物的构成自然界的重要物质.请回答下列问题: