题目内容
15.设NA为阿伏加德罗常数的值.下列叙述不正确的是( )| A. | 常温下,1mol氩气含有的原子数一定为NA | |
| B. | 标准状况下,2.24L Cl2与过量稀NaOH溶液完全反应,转移电子总数为0.1NA | |
| C. | 56g铁片与足量浓硫酸共热反应生成NA个SO2分子 | |
| D. | 常温下,1L pH=12的Na2CO3溶液中含有CO32-的数目大于0.01NA |
分析 A.氩气为单原子分子;
B.氯气与氢氧化钠反应为歧化反应,1mol氯气反应转移1mol电子;
C.铁只能和浓硫酸反应生成硫酸铁和二氧化硫,2mol铁失去6mol电子生成3mol二氧化硫;
D.碳酸根离子为弱酸根离子,水溶液中部分水解.
解答 解:A.氩气为单原子分子,常温下,1mol氩气含有的原子数一定为NA,故A正确;
B.氯气与氢氧化钠反应为歧化反应,1mol氯气反应转移1mol电子,则标准状况下,2.24L Cl2与过量稀NaOH溶液完全反应,转移电子总数为0.1NA,故B正确;
C.56g铁片与足量浓硫酸共热反应生成1.5NA个SO2分子,故C错误;
D.因为溶液的PH=12,c(OH-)=0.01mol/L,n(OH-)=0.01mol,它是由CO32-离子水解产生的:CO32-+H2O?HCO3-+OH-,而CO32-只是部分水解,所以n(CO32-)>0.01mol,故D正确;
故选:C.
点评 本题考查了阿伏伽德罗常数的有关计算,应注意掌握公式的运用和物质的结构,注意盐类水解性质及规律,题目难度中等.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案
相关题目
6.未来可再生能源和清洁能源将成为人类利用新能源的主力军,下列关于能源的叙述正确的是( )
| A. | 化石燃料是可再生能源 | B. | 风能、太阳能是清洁能源 | ||
| C. | 化石燃料都是清洁能源 | D. | 氢能是不可再生的清洁能源 |
7.化学与生产、生活及环境密切相关,下列有关说法正确的是( )
| A. | 工业上海水提镁涉及的一系列反应都是氧化还原反应 | |
| B. | 汽车尾气污染物中含有的氮氧化物,是汽油或柴油不完全燃烧造成的 | |
| C. | 江河入海口形成的三角洲与胶体聚沉有关 | |
| D. | 用于光缆通信的光导纤维和制作航天服的聚酯纤维都是新型无机非金属材料 |
3.在一定温度下容积不变的容器中能说明反应:C(s)+H2O(g)?CO(g)+H2(g) 达到化学平衡状态的是( )
①气体的压强不变
②每生成n个CO分子同时生成n个H2分子
③四种物质的分子数之比为1:1:1:1
④气体的密度不变
⑤断裂2n个H-O键同时断裂n个H-H键
⑥气体的平均摩尔质量不变.
①气体的压强不变
②每生成n个CO分子同时生成n个H2分子
③四种物质的分子数之比为1:1:1:1
④气体的密度不变
⑤断裂2n个H-O键同时断裂n个H-H键
⑥气体的平均摩尔质量不变.
| A. | ①④⑤⑥ | B. | ②⑤⑥ | C. | ①⑤⑥ | D. | ①②④⑤⑥ |
10.下列有关元素周期表的说法正确的是( )
| A. | 第IA的元素全部是金属元素 | |
| B. | 元素周期表有18个族 | |
| C. | 元素周期表含元素最多的族是第ⅢB族 | |
| D. | 短周期是指第一、二、三、四周期 |
20.氮氧化物与悬浮在大气中的食盐粒子相互反应:
4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g)在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol.下列叙述中正确的是( )
4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g)在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol.下列叙述中正确的是( )
| A. | 10min内NaCl浓度变化表示的速率v(NaCl)=0.005 mol•L-1•min-1 | |
| B. | 若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于50% | |
| C. | 若升高温度,平衡逆向移动,则该反应的△H>0 | |
| D. | 若起始时向容器中充入0.2molNO2(g)、0.1molNO(g)和0.1molCl2(g)(固体物质足量),则反应将向正反应方向进行 |
7.下列反应中浓硫酸只表现强氧化性的是( )
| A. | 2NH3+H2SO4(浓)═(NH4)2SO4 | |
| B. | C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O | |
| C. | Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O | |
| D. | 2FeO+4H2SO4(浓)═Fe2(SO4)3+SO2↑+4H2O |
4.下列说法不正确的是( )
| A. | Penguinone分子 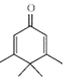 所有碳原子不可能都在同一个平面上 所有碳原子不可能都在同一个平面上 | |
| B. | 1mol  分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol | |
| C. | 醋酸和软脂酸互为同系物,C5H12和C9H20也一定互为同系物 | |
| D. | 石油的裂化、裂解属于化学变化,煤的气化、液化则属于物理变化 |
5.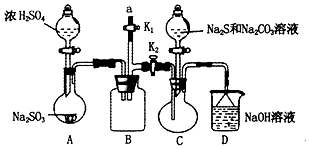 硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.
硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.
(1)实验开始的步骤,组装好仪器检查装置气密性,按图示加入试剂,关闭K1打开K2,先向C中烧瓶加入Na2S和 Na2S2O3混合溶液,再向A中烧瓶滴加浓H2SO4.
(2)C中的烧瓶发生如下反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,反应开始后,C中先有浑浊产生,后又变澄清,此浑浊物是硫;为了保证Na2S2O3的产量,实验中通入C的SO2不能过量,用离子方程式表示其原因S2O32-+2H+=S↓+SO2↑+H2O.
(3)该实验制得的产品中含有NaSO4杂质,为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验开始的步骤进行了改进,改进后的操作是先向A中烧瓶滴加浓H2SO4,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3溶液.
(4)B装置可以起到安全瓶,防止倒吸的作用,另外在实验结束后拆除装置时还可以防止污染空气,具体操作方法是在a处连接盛NaOH溶液的注射器,再关闭K2打开K1.
(5)制取Na2S2O3的另一种方法是直接将硫粉和亚硫酸钠,数混合共热制取.为探究制取硫代硫酸钠最佳条件,设计如下对比实验(每次实验时亚硫酸钠质量均为63g,反应时间为30min):
①实验1、2的目的是探究亚硫酸钠浓度 对亚硫酸钠转化率的影响;
②若要完成表中列出的各项条件对亚硫酸钠转化率的影响探究,除实验1、2外,至少还需进行 次对比实验;
③实验表明:亚硫酸钠转化率不受硫粉质量多少的影响.原因为.硫为固体,不影响化学平衡的移动.
 硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.
硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.(1)实验开始的步骤,组装好仪器检查装置气密性,按图示加入试剂,关闭K1打开K2,先向C中烧瓶加入Na2S和 Na2S2O3混合溶液,再向A中烧瓶滴加浓H2SO4.
(2)C中的烧瓶发生如下反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2,反应开始后,C中先有浑浊产生,后又变澄清,此浑浊物是硫;为了保证Na2S2O3的产量,实验中通入C的SO2不能过量,用离子方程式表示其原因S2O32-+2H+=S↓+SO2↑+H2O.
(3)该实验制得的产品中含有NaSO4杂质,为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验开始的步骤进行了改进,改进后的操作是先向A中烧瓶滴加浓H2SO4,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3溶液.
(4)B装置可以起到安全瓶,防止倒吸的作用,另外在实验结束后拆除装置时还可以防止污染空气,具体操作方法是在a处连接盛NaOH溶液的注射器,再关闭K2打开K1.
(5)制取Na2S2O3的另一种方法是直接将硫粉和亚硫酸钠,数混合共热制取.为探究制取硫代硫酸钠最佳条件,设计如下对比实验(每次实验时亚硫酸钠质量均为63g,反应时间为30min):
| 实验序号 | 溶液pH | 亚硫酸钠与水的质量比 | 反应温度 | 硫粉质量 | 亚硫酸钠转化率 |
| 1 | 10 | 1.5:1 | 100℃ | 18 | 80.7% |
| 2 | 10 | 1.1:1 | 100℃ | 18 | 94.6% |
②若要完成表中列出的各项条件对亚硫酸钠转化率的影响探究,除实验1、2外,至少还需进行 次对比实验;
③实验表明:亚硫酸钠转化率不受硫粉质量多少的影响.原因为.硫为固体,不影响化学平衡的移动.