题目内容
2.(1)城市饮用水处理时可用二氧化氯(ClO2)替代传统的净水剂Cl2.工业上可用Cl2氧化NaClO2溶液制取ClO2.写出该反应的离子方程式Cl2+ClO2-=2ClO2+2Cl-.(2)某地污水中的有机污染物主要成分是三氯乙烯(C2HCl3),向此污水中加入KMnO4(高锰酸钾的还原产物为MnO2)溶液可将其中的三氯乙烯除去,氧化产物只有CO2,写出该反应的化学方程式2KMnO4+C2HCl3═2KCl+2CO2↑+2MnO2+HCl.
分析 (1)Cl2氧化NaClO2溶液制取ClO2,本身被还原为氯离子;
(2)依据题干信息结合原子个数守恒确定产物,再根据氧化还原反应中得失电子数相等结合原子守恒配平写出方程式.
解答 解:(1)Cl2氧化NaClO2溶液制取ClO2,本身被还原为氯离子,离子方程式为:Cl2+ClO2-=2ClO2+2Cl-;
故答案为:Cl2+ClO2-=2ClO2+2Cl-;
(2)由题意可知:KMnO4溶液与三氯乙烯反应,产物有MnO2,CO2,依据原子个数守恒可知其余产物为:KCl,HCl,该反应为氧化还原反应,KMnO4→MnO2,Mn元素由+7价→+4价,一个KMnO4分子得3个电子;C2HCl3→CO2,C元素由+1价→+4价,一个C2HCl3失去6个电子,依据得失电子守恒可知反应的方程式为:2KMnO4+C2HCl3═2KCl+2CO2↑+2MnO2+HCl;
故答案为:2KMnO4+C2HCl3═2KCl+2CO2↑+2MnO2+HCl.
点评 本题以含氯化合物为载体考查氧化还原反应知识,侧重于学生的分析能力的考查,注意抓住题干信息,依据氧化还原反应规律,题目难度中等.

练习册系列答案
相关题目
12.如表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下列化合物与氯化氢加成时,取代基对速率的影响与表中规律类似,其中反应速率最快的是A(填序号).
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
CH2=CHCH2CH3+H2O$\stackrel{H+}{→}$CH3CH(OH)CH2CH3+CH3CH2CH2CH2OH
(主要产物) (次要产物)
请写出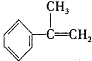 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式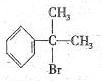 .
.
(3)禽流感在全球的蔓延,使人们谈“禽”色变.从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物.
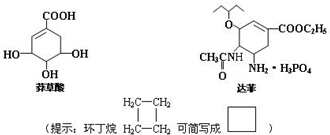
a.莽草酸分子中含有的官能团有羧基、羟基、碳碳双键;
b.莽草酸在浓硫酸作用下加热可以得到B(B的结构简式为: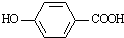 ),其反应类型为:消去反应;
),其反应类型为:消去反应;
c.请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):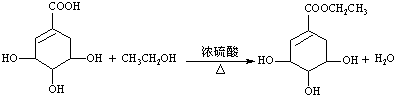 .
.
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
CH2=CHCH2CH3+H2O$\stackrel{H+}{→}$CH3CH(OH)CH2CH3+CH3CH2CH2CH2OH
(主要产物) (次要产物)
请写出
 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式 .
.(3)禽流感在全球的蔓延,使人们谈“禽”色变.从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物.

a.莽草酸分子中含有的官能团有羧基、羟基、碳碳双键;
b.莽草酸在浓硫酸作用下加热可以得到B(B的结构简式为:
 ),其反应类型为:消去反应;
),其反应类型为:消去反应;c.请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):
 .
.
13.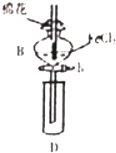 某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
I.先向B中的FeCl2溶液(约10ml)中通入Cl2,当B的溶液变黄时,停止通气
Ⅱ.打开活寒b,使约2ml的溶液流入D试管中,检验D溶液中的离子
Ⅲ.接着再向B中通入一定量的SO2气体
IV.更新试管D,重复过程Ⅱ,检验取出溶液中的离子
(1)仪器B的名称是分液漏斗,棉花中浸润的溶液为NaOH溶液的是吸收Cl2、SO2,防尾气污染环境
(2)实验室制备氯气的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,反应中消耗4molHCl,转移的电子数是2NA
(3)过程Ⅲ中一定发生反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.过程ⅠV中检验取出溶液中足否含有硫酸根的操作是取溶液少许于试管中,先加入足量稀盐酸酸化,再滴加少量BaCl2溶液,若有白色沉淀生成,证明有SO42-,反之无
(4)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,其中一定能够证明SO、Fe2+和Cl-还原性强弱关系的是乙、丙:则SO2、Fe2+和Cl-还原性强弱顺序是SO2>Fe2+>Cl-
 某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:I.先向B中的FeCl2溶液(约10ml)中通入Cl2,当B的溶液变黄时,停止通气
Ⅱ.打开活寒b,使约2ml的溶液流入D试管中,检验D溶液中的离子
Ⅲ.接着再向B中通入一定量的SO2气体
IV.更新试管D,重复过程Ⅱ,检验取出溶液中的离子
(1)仪器B的名称是分液漏斗,棉花中浸润的溶液为NaOH溶液的是吸收Cl2、SO2,防尾气污染环境
(2)实验室制备氯气的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,反应中消耗4molHCl,转移的电子数是2NA
(3)过程Ⅲ中一定发生反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.过程ⅠV中检验取出溶液中足否含有硫酸根的操作是取溶液少许于试管中,先加入足量稀盐酸酸化,再滴加少量BaCl2溶液,若有白色沉淀生成,证明有SO42-,反之无
(4)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,其中一定能够证明SO、Fe2+和Cl-还原性强弱关系的是乙、丙:则SO2、Fe2+和Cl-还原性强弱顺序是SO2>Fe2+>Cl-
| 过程Ⅱ中检出离子 | 过程ⅠV中检出离子 | |
| 甲 | 有 Fe3+无 Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有S042- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
17.下列属于吸热反应同时又属于氧化还原反应的是( )
| A. | 点燃的镁条在二氧化碳中继续燃烧 | B. | Ca(OH)2与NH4Cl的反应 | ||
| C. | 灼热的碳与二氧化碳的反应 | D. | 酸碱中和反应 |
7.下列过程没有发生化学反应的是( )
| A. | 用食醋除去暖水瓶中的薄层水垢 | B. | 石油的分馏和煤的干馏 | ||
| C. | 用二氧化氯(ClO2)为自来水消毒 | D. | 液氨作制冷剂 |
14.化学与科学、技术、生产、生活密切相关.下列有关说法中不正确的是( )
| A. | “血液透析”利用了胶体的性质 | |
| B. | 华裔科学家高琨因在光纤传输信息领域中取得突破性成就而获得诺贝尔奖,光纤的主要成分是高纯度的二氧化硅 | |
| C. | 玻璃钢是一种合金,广泛用于汽车车身 | |
| D. | 只要符合限量,“亚硝酸盐”、“食用色素”、“苯甲酸钠”可以作为某些食品的添加剂 |
11.有100mL3mol•L-1的NaOH溶液和100mL1mol•L-1的AlCl3溶液.
(a)将NaOH溶液逐滴滴加到AlCl3溶液中,边滴边振荡,直至滴完;
(b)将AlCl3逐滴滴加到NaOH溶液中,边滴边振荡,直至滴完;
对上述实验所得出的结论正确的是( )
(a)将NaOH溶液逐滴滴加到AlCl3溶液中,边滴边振荡,直至滴完;
(b)将AlCl3逐滴滴加到NaOH溶液中,边滴边振荡,直至滴完;
对上述实验所得出的结论正确的是( )
| A. | 现象相同,沉淀质量相等 | B. | 现象相同,沉淀质量不相等 | ||
| C. | 现象不相同,沉淀质量相等 | D. | 现象不相同,沉淀质量不相等 |
12.下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
| A. | 在标准状况下,22.4L水所含分子数目为NA | |
| B. | 1mol.L-1 K2SO4溶液所含K+数目为2NA | |
| C. | 1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA | |
| D. | O2的摩尔体积约为22.4L.mol-1 |