题目内容
下列有关说法正确的是( )
A、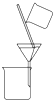 不可除去乙醇中的苯酚 |
B、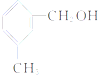 遇FeCl3溶液可显紫色 |
| C、苯酚钠溶液中通入少量二氧化碳生成碳酸钠 |
D、苯酚与Na2CO3溶液反应的离子方程式为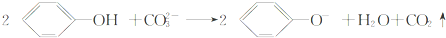 |
考点:过滤、分离与注入溶液的仪器,有机物的结构和性质,苯酚的化学性质
专题:
分析:A.乙醇与苯酚互溶;
B.酚类遇氯化铁显紫色;
C.苯酚的酸性强于碳酸氢根离子,苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠;
D. 酸性比H2CO3弱,
酸性比H2CO3弱, 酸性大于HCO3-,此反应不会生成二氧化碳.
酸性大于HCO3-,此反应不会生成二氧化碳.
B.酚类遇氯化铁显紫色;
C.苯酚的酸性强于碳酸氢根离子,苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠;
D.
 酸性比H2CO3弱,
酸性比H2CO3弱, 酸性大于HCO3-,此反应不会生成二氧化碳.
酸性大于HCO3-,此反应不会生成二氧化碳.解答:
解:A.乙醇与苯酚互溶,无法用过滤的方法分离,应用蒸馏的方法分离,故A正确;
B. 属于芳香醇,不属于酚类,故和氯化铁没有紫色现象,故B错误;
属于芳香醇,不属于酚类,故和氯化铁没有紫色现象,故B错误;
C.苯酚钠与二氧化碳反应生成的是苯酚和碳酸氢钠,不是生成碳酸钠,故C错误;
D. 酸性比H2CO3弱,
酸性比H2CO3弱, 酸性大于HCO3-,反应离子方程式:C6H5OH+CO32-=C6H5O-+HCO3-,不会生成二氧化碳,故D错误;
酸性大于HCO3-,反应离子方程式:C6H5OH+CO32-=C6H5O-+HCO3-,不会生成二氧化碳,故D错误;
故选A.
B.
 属于芳香醇,不属于酚类,故和氯化铁没有紫色现象,故B错误;
属于芳香醇,不属于酚类,故和氯化铁没有紫色现象,故B错误;C.苯酚钠与二氧化碳反应生成的是苯酚和碳酸氢钠,不是生成碳酸钠,故C错误;
D.
 酸性比H2CO3弱,
酸性比H2CO3弱, 酸性大于HCO3-,反应离子方程式:C6H5OH+CO32-=C6H5O-+HCO3-,不会生成二氧化碳,故D错误;
酸性大于HCO3-,反应离子方程式:C6H5OH+CO32-=C6H5O-+HCO3-,不会生成二氧化碳,故D错误;故选A.
点评:本题考查苯酚性质,注意酚类和芳香醇的区别,难度不大.

练习册系列答案
相关题目
将0.2mol?L-1Ba(OH)2溶液与0.05mol?L-1NaHSO4溶液等体积混合后,下列几种离子浓度大小顺序正确的是( )
| A、c(Ba2+)>c(OH-)>c(Na+)>c(SO42-) |
| B、c(Na+)>c(OH-)>c(Ba2+)>c(SO42-) |
| C、c(Na+)>c(Ba2+)>c(OH-)>c(SO42-) |
| D、c(OH-)>c(Ba2+)>c(Na+)>c(SO42-) |
用质量均为100g的Cu作电极,电解AgNO3溶液.稍电解一段时间后,两电极的质量相差28g,此时两电极的质量分别为( )
| A、阳极100 g,阴极128 g |
| B、阳极93.6 g,阴极121.6 g |
| C、阳极91.0 g,阴极119.0 g |
| D、阳极86.0 g,阴极114.0 g |
25℃时,有关弱酸的电离平衡常数如下,下列有关说法正确的是( )
| 弱酸的化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 18×10-5 | 4.5×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2CO3)>pH(NaCN) |
| B、a mol?L-1HCN溶液与b mol?L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| C、向0.1 mol?L-1CH3COOH溶液中逐滴加水,则醋酸的电离程度增大、c(H+)减小 |
| D、NaHCO3和Na2CO3混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
下列实验操作中,用于分离食用油和氯化钠溶液的最佳方案是( )
A、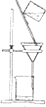 |
B、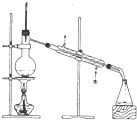 |
C、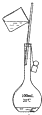 |
D、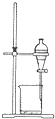 |
将同体积同物质的量浓度的AgNO3溶液中的Ag+完全沉淀,则需同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液的体积比为( )
| A、1:2:3 |
| B、3:2:1 |
| C、1:1:1 |
| D、6:3:2 |
为减少新鲜蔬菜中的维生素C的流失,下列有关烹调蔬菜的方法不妥当的是( )
| A、蔬菜最好洗干净后再切 |
| B、炒蔬菜的时间不能太长,炒熟即可 |
| C、新鲜蔬菜应放在冰箱中储存 |
| D、把蔬菜放在高压锅中焖煮 |
“低碳经济”是以低能耗、低污染、低排放为基础的可持续发展经济模式.下列说法与“低碳经济”不符合的是( )
| A、大力研发新型有机溶剂替代水作为萃取剂 |
| B、加强对煤、石油、天然气等综合利用的研究,提高燃料的利用率 |
| C、利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 |
| D、使用甲醇、乙醇混合型汽油可以减少对大气的污染 |