题目内容
5.已知Ba(OH)2•8H2O与NH4Cl(s)反应的焓变为△H1,Ba(OH)2•8H2O分解的热焓变为△H2,Ba(OH)2与NH4Cl(s)反应的热焓变△H3<0.则( )| A. | △H1<0 | B. | △H1>△H2 | C. | △H2═△H1+△H3 | D. | △H2>|△H3| |
分析 Ba(OH)2•8H2O与NH4Cl(s)反应的焓变为△H1,是吸热反应,所以△H1>0,Ba(OH)2•8H2O分解是吸热反应,所以的热焓变为△H2>0,而Ba(OH)2•8H2O与NH4Cl(s)反应可以当作Ba(OH)2•8H2O第一步发生分解;第二步Ba(OH)2与NH4Cl(s)反应,所以根据盖斯定律,△H1=△H2+△H3,由此分析解答.
解答 解:A、Ba(OH)2•8H2O与NH4Cl(s)反应的焓变为△H1,是吸热反应,所以△H1>0,故A错误;
B、由△H1=△H2+△H3和△H3<0,所以△H1<△H2,故B错误;
C、根据盖斯定律,△H1=△H2+△H3,而不是△H2═△H1+△H3,故C错误;
D、由△H1=△H2+△H3,得-△H3=△H2-△H1,即|△H3|=△H2-△H1,又因为△H1>0,所以△H2>|△H3|,故D正确;
故选D.
点评 本题涉及盖斯定律的应用以及反应热的判断,属于基本知识的考查,难度不大.

练习册系列答案
相关题目
9.下列反应中会有沉淀产生的是( )
| A. | 将二氧化硫气体通入酸性KMnO4溶液中 | |
| B. | 将二氧化硫气体通入碘水中 | |
| C. | 将二氧化硫气体通入BaCl2溶液中 | |
| D. | 将少量二氧化硫气体通入Ba(OH)2溶液中 |
16.下列实验装置图正确的是( )
| A. | 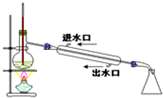 工业乙醇的蒸馏 | B. | 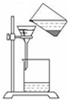 苯甲酸趁热过滤 | ||
| C. | 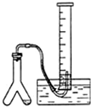 制少量乙炔并测体积 | D. | 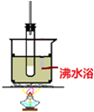 实验室制硝基苯 |
20.下列用连线方法对部分化学知识进行归纳的内容中,有错误的组是( )
| A. | 保护环境:控制“白色污染”--减少和控制使用所有塑料制品防止水的污染--提倡使用无磷洗衣粉 | |
| B. | 基本安全常识:饮用假酒中毒--由甲醇引起食用假盐中毒--由亚硝酸钠引起 | |
| C. | 物质的性质与用途:磺胺类药物能抑制细菌合成核酸--治疗肺炎、脑膜炎、呼吸道感染酸能与碱中和-----胃酸过多的病人服用含氢氧化钠的药物 | |
| D. | 生活中的一些做法:除去衣服上的油污--可用汽油洗涤使煤燃烧更旺--可增大煤与空气接触面积 |
14.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | 质量数为37的氯原子:$\stackrel{17}{37}$Cl | B. | H2O的结构式:H-O-H | ||
| C. | CH4分子的比例模型: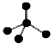 | D. | 氯化铵的电子式: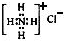 |
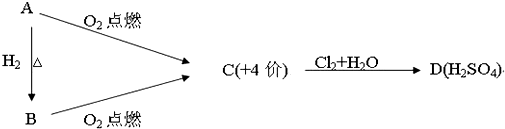
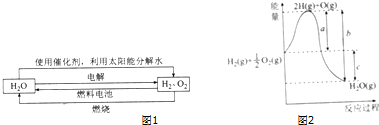 科学家认为氢气是一种高效且无污染的理想能源,近20年来,以氢气为未来的动力燃料的研究获得了迅速发展.
科学家认为氢气是一种高效且无污染的理想能源,近20年来,以氢气为未来的动力燃料的研究获得了迅速发展.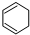 $\stackrel{Br_{2}}{→}$A$→_{△}^{H_{2}/Ni}$B$\stackrel{NaOH溶液}{→}$
$\stackrel{Br_{2}}{→}$A$→_{△}^{H_{2}/Ni}$B$\stackrel{NaOH溶液}{→}$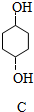 $\stackrel{O_{2}/Cu}{→}$
$\stackrel{O_{2}/Cu}{→}$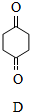
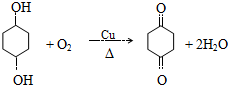 .
. .
.