题目内容
火电厂排放气体中含有二氧化硫、氮氧化物等大气污染物,大气污染物的研究治理对改善环境具有重要意义.
(1)煤燃烧产生的烟气(含有氮氧化物、SO2、PM2.5等),直接排放到空气中,引发的主要环境问题有 .(填写字母编号)
A.水体富营养化 B.重金属污染 C.雾霾 D.酸雨
(2)将含有SO2的废气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,在废气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间的二氧化碳,以增加其脱硫效率;脱硫时控制浆液的pH值,此时浆液含有的亚硫酸氢钙可以被氧气快速氧化生成硫酸钙.写出亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式: .
(3)有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,工艺流程如图:A的化学式为 ,若生成ag A,理论上可以回收SO2的质量为 g.
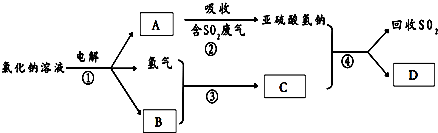
(4)汽车尾气中含有的氮氧化物(NOx)能形成酸雨,写出NO2转化为HNO3的化学方程式 .当尾气中空气不足时,NOX在催化转化器中被还原成N2排出,写出NO被CO还原的化学方程式 .
(5)工业上常用Na2CO3溶液处理煤燃烧产生的烟气,写出SO2、NO与Na2CO3溶液反应生成Na2SO4、N2的离子方程式 .
(1)煤燃烧产生的烟气(含有氮氧化物、SO2、PM2.5等),直接排放到空气中,引发的主要环境问题有
A.水体富营养化 B.重金属污染 C.雾霾 D.酸雨
(2)将含有SO2的废气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,在废气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间的二氧化碳,以增加其脱硫效率;脱硫时控制浆液的pH值,此时浆液含有的亚硫酸氢钙可以被氧气快速氧化生成硫酸钙.写出亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式:
(3)有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,工艺流程如图:A的化学式为

(4)汽车尾气中含有的氮氧化物(NOx)能形成酸雨,写出NO2转化为HNO3的化学方程式
(5)工业上常用Na2CO3溶液处理煤燃烧产生的烟气,写出SO2、NO与Na2CO3溶液反应生成Na2SO4、N2的离子方程式
考点:二氧化硫的污染及治理,常见的生活环境的污染及治理
专题:元素及其化合物,化学应用
分析:(1)煤燃烧产生的烟气中含有二氧化硫、二氧化碳以及粉尘等,都可导致环境污染;
(2)CO2与CaCO3反应生成易溶的Ca(HCO3)2,亚硫酸氢钙具有还原性,可被氧化为硫酸钙;
(3)依据流程图分析,电解氯化钠溶液得到氢气、氯气、氢氧化钠溶液,B为Cl2,氯气和氢气反应生成C为HCl,A为NaOH,和二氧化硫反应生成亚硫酸氢钠,盐酸和亚硫酸氢钠反应生成氯化钠、二氧化硫和水;
(4)二氧化氮和水反应生成硝酸和一氧化氮;NO被CO还原,则CO被NO氧化生成二氧化碳,据此写出反应方程式;
(5)二氧化硫具有还原性被氧化为硫酸,一氧化氮具有氧化性被还原为氮气,依据原子守恒书写;
(2)CO2与CaCO3反应生成易溶的Ca(HCO3)2,亚硫酸氢钙具有还原性,可被氧化为硫酸钙;
(3)依据流程图分析,电解氯化钠溶液得到氢气、氯气、氢氧化钠溶液,B为Cl2,氯气和氢气反应生成C为HCl,A为NaOH,和二氧化硫反应生成亚硫酸氢钠,盐酸和亚硫酸氢钠反应生成氯化钠、二氧化硫和水;
(4)二氧化氮和水反应生成硝酸和一氧化氮;NO被CO还原,则CO被NO氧化生成二氧化碳,据此写出反应方程式;
(5)二氧化硫具有还原性被氧化为硫酸,一氧化氮具有氧化性被还原为氮气,依据原子守恒书写;
解答:
解:(1)煤燃烧的产物中含有氮氧化物、SO2、PM2.5等分别导致雾霾、酸雨、粉尘污染等,没有营养元素排入水中,不会引起水体富营养化,无重金属污染;
故答案为:CD;
(2)亚硫酸氢钙具有还原性,可被氧化为硫酸钙,反应的方程式为Ca( HSO3)2+O2=CaSO4+H2SO4,故答案为:Ca( HSO3)2+O2=CaSO4+H2SO4;
(3)依据流程图分析,电解氯化钠溶液得到氢气、氯气、氢氧化钠溶液,B为Cl2,氯气和氢气反应生成C为HCl,A为NaOH,和二氧化硫反应生成亚硫酸氢钠,盐酸和亚硫酸氢钠反应生成氯化钠、二氧化硫和水,若生成ag A为NaOH物质的量=
,理论上可以回收SO2的质量依据化学方程式计算,SO2+NaOH=NaHSO3,二氧化硫质量=
×64g/mol=1.6ag;
故答案为:NaOH,1.6a;
(4)二氧化氮和水反应生成硝酸和一氧化氮,反应方程式为:3NO2+H2O=2HNO3+NO,在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:2CO+2NO
N2+2CO2;
故答案为:3NO2+H2O═2HNO3+NO,2NO+2CO
N2+2CO2;
(5)工业上常用Na2CO3溶液处理煤燃烧产生的烟气,二氧化硫具有还原性被氧化为硫酸,一氧化氮具有氧化性被还原为氮气,写出SO2、NO与Na2CO3溶液反应生成Na2SO4、N2的离子方程式:2SO2 +2NO+2CO32-=2SO42-+N2 +CO2;
故答案为:2SO2 +2NO+2CO32-=2SO42-+N2 +CO2.
故答案为:CD;
(2)亚硫酸氢钙具有还原性,可被氧化为硫酸钙,反应的方程式为Ca( HSO3)2+O2=CaSO4+H2SO4,故答案为:Ca( HSO3)2+O2=CaSO4+H2SO4;
(3)依据流程图分析,电解氯化钠溶液得到氢气、氯气、氢氧化钠溶液,B为Cl2,氯气和氢气反应生成C为HCl,A为NaOH,和二氧化硫反应生成亚硫酸氢钠,盐酸和亚硫酸氢钠反应生成氯化钠、二氧化硫和水,若生成ag A为NaOH物质的量=
| ag |
| 40g/mol |
| ag |
| 40g/mol |
故答案为:NaOH,1.6a;
(4)二氧化氮和水反应生成硝酸和一氧化氮,反应方程式为:3NO2+H2O=2HNO3+NO,在催化剂条件下,一氧化碳被氧化生成二氧化碳,一氧化氮被还原生成氮气,所以其反应方程式为:2CO+2NO
| ||
故答案为:3NO2+H2O═2HNO3+NO,2NO+2CO
| ||
(5)工业上常用Na2CO3溶液处理煤燃烧产生的烟气,二氧化硫具有还原性被氧化为硫酸,一氧化氮具有氧化性被还原为氮气,写出SO2、NO与Na2CO3溶液反应生成Na2SO4、N2的离子方程式:2SO2 +2NO+2CO32-=2SO42-+N2 +CO2;
故答案为:2SO2 +2NO+2CO32-=2SO42-+N2 +CO2.
点评:本题涉及化学反应方程式书写方法、化学方程式计算应用等知识点,注意化学方程式的计算方法,为易错点.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
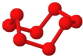
观察下列模型并结合有关信息,判断有关说法正确的是( )
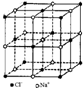
| 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl | |
| 结构模型示意图 |  |
 |
 |
 |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
| A、单质硼属分子晶体,其结构单元B12中含有30个B-B键,含20个正三角形 |
| B、SF6是由极性键构成的分子 |
| C、固态硫S8属于原子晶体 |
| D、NaCl熔化和溶于水均能产生自由移动的离子,且破坏的是同种作用力,NaCl晶胞中每个Na+周围最近且等距离的Na+有6个 |
下列化学用语正确的是( )
A、中子数为8的碳原子:
| ||
B、氟离子的结构示意图: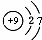 | ||
C、甲烷分子的结构式: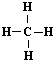 | ||
D、N2的电子式: |
下列有关物质性质的说法错误的是( )
| A、热稳定性:HCl>HI |
| B、原子半径:Na>Mg |
| C、酸性:H2SO3>H2SO4 |
| D、结合质子能力:S2->Cl- |
已知:①H2O(g)═H2O(l)△H=-Q1 kJ?mol-1
②C2H5OH(g)═C2H5OH(l)△H=-Q2 kJ?mol-1
③C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=-Q3 kJ?mol-1
下列判断正确是( )
②C2H5OH(g)═C2H5OH(l)△H=-Q2 kJ?mol-1
③C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=-Q3 kJ?mol-1
下列判断正确是( )
| A、酒精的燃烧热△H=-Q3 kJ?mol-1 |
| B、由③可知1mol C2H5OH(g)的能量高于2mol CO2(g)和3mol H2O(g)的总能量 |
| C、H2O(g)→H2O(l)释放出了热量,所以该过程为放热反应 |
| D、23g液体酒精完全燃烧生成CO2(g)和H2O(l),释放出的热量为(0.5Q3-0.5Q2+1.5Q1)kJ |
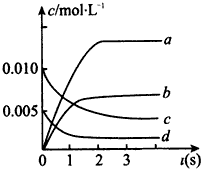 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表所示
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表所示