题目内容
如图所示的物质转化关系中(反应条件未全部列出),A为某金属矿的主要成分,B、D为组成元素相同的无色液体,C、E是单质,I的溶液呈蓝色,反应①是工业上冶炼金属的一种方法.
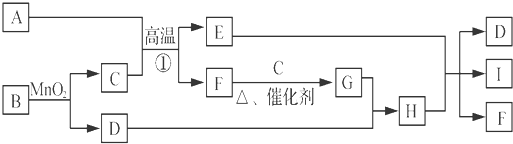
请回答下列问题:
(1)B的电子式为 .
(2)G的化学式为 .
(3)E与H的浓溶液反应的化学方程式为 .
(4)I的溶液与氢氧化钠溶液反应的离子方程式为 .

请回答下列问题:
(1)B的电子式为
(2)G的化学式为
(3)E与H的浓溶液反应的化学方程式为
(4)I的溶液与氢氧化钠溶液反应的离子方程式为
考点:无机物的推断
专题:
分析:B、D为组成元素相同的无色液体,且B在二氧化锰作用下生成D与单质C,可知B为H2O2,D为H2O,则C为O2,反应①是工业上冶炼金属的一种方法,由I的溶液呈蓝色,可知A中应含有Cu元素,应为Cu2S,则E为Cu,F为SO2,G为SO3,H为H2SO4,I为CuSO4,据此答题.
解答:
解:B、D为组成元素相同的无色液体,且B在二氧化锰作用下生成D与单质C,可知B为H2O2,D为H2O,则C为O2,反应①是工业上冶炼金属的一种方法,由I的溶液呈蓝色,可知A中应含有Cu元素,应为Cu2S,则E为Cu,F为SO2,G为SO3,H为H2SO4,I为CuSO4,
(1)由以上分析可知,B为H2O2,电子式为 ,故答案为:
,故答案为: ;
;
(2)由上述分析可知,G为SO3,故答案为:SO3;
(3)Cu与浓硫酸反应的化学方程式为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓
)CuSO4+SO2↑+2H2O;
(4)CuSO4溶液与氢氧化钠溶液反应的离子方程式为:Cu2++2OH-=Cu(OH)2↓,
故答案为:Cu2++2OH-=Cu(OH)2↓.
(1)由以上分析可知,B为H2O2,电子式为
 ,故答案为:
,故答案为: ;
;(2)由上述分析可知,G为SO3,故答案为:SO3;
(3)Cu与浓硫酸反应的化学方程式为:Cu+2H2SO4(浓)
| ||
故答案为:Cu+2H2SO4(浓
| ||
(4)CuSO4溶液与氢氧化钠溶液反应的离子方程式为:Cu2++2OH-=Cu(OH)2↓,
故答案为:Cu2++2OH-=Cu(OH)2↓.
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力和推断能力的考查,需要学生熟练掌握元素化合物知识,化学推断题是一类综合性较强的试题,常涉及元素及化合物性质、化学反应原理、环境保护、化学计算等知识,根据物质的特殊颜色或特殊化学反应进行推断.

练习册系列答案
相关题目
下列实验能成功的是( )
①用水鉴别Na2CO3和NaHCO3固体;
②用观察法区别Na2O和Na2O2;
③用MgCl2溶液鉴别Na2CO3溶液和NaOH溶液;
④用稀盐酸鉴别Na2CO3溶液和NaHCO3溶液.
①用水鉴别Na2CO3和NaHCO3固体;
②用观察法区别Na2O和Na2O2;
③用MgCl2溶液鉴别Na2CO3溶液和NaOH溶液;
④用稀盐酸鉴别Na2CO3溶液和NaHCO3溶液.
| A、①②③④ | B、①② |
| C、②③ | D、①②④ |
已知某有机物X的结构简式如图所示,下列有关叙述不正确的是( )


| A、X的化学式为C10H10O6 |
| B、X在一定条件下能与FeCl3溶液发生显色反应 |
| C、1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol |
| D、X在一定条件下能发生消去反应和酯化反应 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
| W | X | |
| Y | Z |
| A、X、Y、Z中最简单氢化物稳定性最弱的是Y |
| B、Z元素氧化物对应水化物的酸性一定强于Y |
| C、X元素形成的单核阴离子还原性强于Y |
| D、Z元素单质在化学反应中只表现氧化性 |
某有机物在酸性条件下可以发生水解反应生成 A,B两种不同物质,而且A,B两种物质的相对分子质量相同,这种有机物可能是( )
| A、乙酸乙酯 | B、甲酸乙酯 |
| C、乙酸甲酯 | D、丙酸乙酯 |
下列关于甲烷性质叙述中正确的是( )
| A、甲烷能使酸性KMnO4溶液的紫色褪去 |
| B、甲烷与足量氯气在光照时有机产物只有四氯化碳 |
| C、甲烷是一种无色无味、难溶于水的气体 |
| D、等物质的量的甲烷和乙烷(C2H6)分别完全燃烧时,甲烷消耗的氧气多 |
下列实验过程中,始终无明显现象的是( )
| A、NH3通人AlCl3溶液中 |
| B、用脱脂棉包裹Na2O2粉末露置在潮湿空气中 |
| C、CO2通入CaCl2溶液中 |
| D、稀盐酸滴加到Fe(OH)3胶体溶液中 |
已知下列反应的热化学方程式为:
C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol
CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H2=-870.3kJ/mol
H2(g)+
O2(g)=H2O(l)△H3=-285.8kJ/mol
2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的反应热△H(焓变)为( )
C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol
CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H2=-870.3kJ/mol
H2(g)+
| 1 |
| 2 |
2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的反应热△H(焓变)为( )
| A、488.3 kJ/mol |
| B、-488.3 kJ/mol |
| C、-244.15 kJ/mol |
| D、244.15 kJ/mol |
