题目内容
过氧化氢(H2O2)又叫双氧水,其水溶液可用于制备工业上的漂白剂、特殊环境里燃料燃烧的助燃剂、医疗上的消毒剂、实验室里的制氧剂等.过氧化钠(Na2O2)可用于制备工业上的漂白剂、实验室里的制氧剂、呼吸面具或潜水艇中的制氧剂等.过氧原子团“02”由2个氧原子共用1对电子形成.
(1)分别写出H2O2、Na2O2的电子式: 、
(2)①H2O、H2O2中化学键的不同点是 .
②Na2O、Na2O2中化学键的不同点是 .
③H202的化合物类型是 (填“共价化合物”或“离子化合物”).
(3)分别写出H202、Na2O2作供氧剂的化学方程式:
H202: .Na202: .
(1)分别写出H2O2、Na2O2的电子式:
(2)①H2O、H2O2中化学键的不同点是
②Na2O、Na2O2中化学键的不同点是
③H202的化合物类型是
(3)分别写出H202、Na2O2作供氧剂的化学方程式:
H202:
考点:化学键,电子式,化学方程式的书写,离子化合物的结构特征与性质
专题:
分析:(1)H2O2、Na2O2分别为共价化合物、离子化合物;
(2)①H2O的结构式为H-O-H,H2O2的结构式为H-O-O-H;
②Na2O中只含离子键,Na2O2中含离子键和O-O非极性键;
③H202中只含共价键;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,过氧化钠与水或二氧化碳反应均生成氧气.
(2)①H2O的结构式为H-O-H,H2O2的结构式为H-O-O-H;
②Na2O中只含离子键,Na2O2中含离子键和O-O非极性键;
③H202中只含共价键;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,过氧化钠与水或二氧化碳反应均生成氧气.
解答:
解:(1)H2O2、Na2O2分别为共价化合物、离子化合物,电子式分别为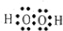 、
、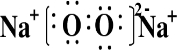 ,
,
故答案为: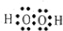 、
、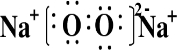 ;
;
(2)①H2O的结构式为H-O-H,H2O2的结构式为H-O-O-H,则不同点为过氧化氢中含非极性键,故答案为:过氧化氢中含非极性键;
②Na2O中只含离子键,Na2O2中含离子键和O-O非极性键,则不同点为过氧化钠中含非极性键,故答案为:过氧化钠中含非极性键;
③H202中只含共价键,则属于共价化合物,故答案为:共价化合物;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,过氧化钠与水或二氧化碳反应均生成氧气,反应分别为2H2O2
2H2O+O2↑、2Na2O2+2H2O═4NaOH+O2↑或2Na2O2+2CO2═2Na2CO3+O2↑,故答案为:2H2O2
2H2O+O2↑;2Na2O2+2H2O═4NaOH+O2↑或2Na2O2+2CO2═2Na2CO3+O2↑.
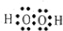 、
、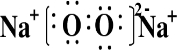 ,
,故答案为:
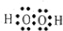 、
、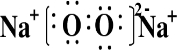 ;
;(2)①H2O的结构式为H-O-H,H2O2的结构式为H-O-O-H,则不同点为过氧化氢中含非极性键,故答案为:过氧化氢中含非极性键;
②Na2O中只含离子键,Na2O2中含离子键和O-O非极性键,则不同点为过氧化钠中含非极性键,故答案为:过氧化钠中含非极性键;
③H202中只含共价键,则属于共价化合物,故答案为:共价化合物;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,过氧化钠与水或二氧化碳反应均生成氧气,反应分别为2H2O2
| ||
| ||
点评:本题考查化学键,为高频考点,把握化学键形成的一般规律及常见物质中的化学键为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
下列实验操作错误的是( )
| A、进行分液操作时,分液漏斗中下层液体从下口放出 上层液体从上口倒出 |
| B、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处 |
| C、进行分液操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| D、进行蒸发操作时,不能使混合物中的水分完全蒸干 |
24mL 0.05mol/L的Na2SO3溶滚,恰好与20mL0.02mol/L的K2Cr2O7溶液完全反应,亚硫酸钠被氧化为Na2SO4,则铬元素在还原产物中的化合价为( )
| A、+6 | B、+3 | C、+2 | D、0 |
下列事实能用电化学原理解释的是( )
| A、银质物品久置表面变暗 |
| B、远洋海轮的尾部装上一定数量的锌板 |
| C、常温条件下,在空气中铝不易被腐蚀 |
| D、用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
下列说法中正确的是( )
| A、共价化合物中一定只含有极性共价键 |
| B、只含有共价键的物质一定是共价化合物 |
| C、离子化合物中可能含有极性共价键或非极性共价键 |
| D、有较强共价键存在的物质熔沸点一定很高 |
用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A、1mol Na2O2固体中含有离子总数为3 NA |
| B、常温常压下,3.2gCH4中含有电子2 NA |
| C、标准状况下,28g N2和CO所组成的混合气体,其体积为22.4L |
| D、足量铁粉与1molCl2在加热条件下充分反应,转移的电子数为3NA |