题目内容
同温同压下,有O2和O3两种气体.
(1)若二者体积相同,则分子数之比为 ;密度之比为 ;所含氧原子数目之比为 .
(2)若二者所含氧原子数目相同时,则它们的体积之比为 .
(1)若二者体积相同,则分子数之比为
(2)若二者所含氧原子数目相同时,则它们的体积之比为
考点:物质的量的相关计算
专题:计算题
分析:同温同压下,Vm相同,
(1)若二者体积相同,由V=nVm可知,则物质的量相同,结合N=nNA、ρ=
及分子构成计算;
(2)若二者所含氧原子数目相同时,则物质的量比为3:2,结合V=nVm计算.
(1)若二者体积相同,由V=nVm可知,则物质的量相同,结合N=nNA、ρ=
| M |
| Vm |
(2)若二者所含氧原子数目相同时,则物质的量比为3:2,结合V=nVm计算.
解答:
解:同温同压下,Vm相同,
(1)若二者体积相同,由V=nVm可知,则物质的量相同,由N=nNA可知,分子数之比为1:1,由ρ=
可知,密度之比为32:48=2:3,由分子构成可知,所含氧原子数目之比为2:3,故答案为:1:1;2:3;2:3;
(2)若二者所含氧原子数目相同时,则物质的量比为3:2,由V=nVm可知,它们的体积之比为3:2,故答案为:3:2.
(1)若二者体积相同,由V=nVm可知,则物质的量相同,由N=nNA可知,分子数之比为1:1,由ρ=
| M |
| Vm |
(2)若二者所含氧原子数目相同时,则物质的量比为3:2,由V=nVm可知,它们的体积之比为3:2,故答案为:3:2.
点评:本题考查物质的量的有关计算,为高频考点,把握气体体积、物质的量及微粒数目、密度的关系为解答的关键,侧重分析能力、计算能力的考查,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
NA表示阿伏加德罗常数,下列说法中不正确的是( )
| A、KIO3+6HI=KI+3H2O+3I2,生成3mol I2转移电子的总数为5NA |
| B、标准状况下,5.6L氧气中含有O的总数为0.5NA |
| C、25℃时,pH=13的Ba(OH)2溶液1.0L中含有OH-总数为0.1NA |
| D、20g重水(D2O)中所含电子总数为8NA |
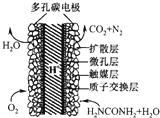 电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )
电化学化学家正在研究尿素动力燃料电池,尿液也能发电.用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电.尿素燃料电池结构如图所示,下列关于该电池描述正确的是( )| A、电池工作时H+移向负极 |
| B、该装置还可以将电能转化成为化学能 |
| C、电池的负极反应式为:CO(NH2)2+H2O-6e-=CO2+N2+6H+ |
| D、理论上电池工作时,每消耗67.2L O2时,可以净化2mol CO(NH2)2 |
下列各项中,两种物质间反应均产生1mol气体时,参加反应的酸的物质的量最少的是( )
| A、碳与浓硝酸 |
| B、铜与浓硫酸 |
| C、锌与稀硫酸 |
| D、二氧化锰与浓盐酸 |
下列各组离子在指定的溶液中可能大量共存的是( )
| A、使甲基橙变红色的溶液:K+、Al3+、MnO4-、C2O42- |
| B、加入铝产生氢气的溶液:H+、Mg2+、NO3-、SO42- |
| C、pH=12的溶液中:Na+、Ba2+、NO3-、Cl- |
| D、含Al2Fe(SO4)4的溶液:Na+、NH4+、S2O32-、ClO- |

 将一定质量的镁铝合金全部溶于100mL某浓度的盐酸中.向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如图所示.则盐酸的物质的量浓度为
将一定质量的镁铝合金全部溶于100mL某浓度的盐酸中.向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如图所示.则盐酸的物质的量浓度为