题目内容
6.某溶液中只含有Na+、Fe3+、Cl-、SO42-四种离子,已知Na+、Fe3+、Cl-的个数比为1:2:3,则溶液中Fe3+和SO42-的个数比为( )| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
分析 设Na+、Fe3+、Cl-的物质的量分别为1mol、2mol、3mol,根据溶液中电荷守恒有3n(Fe3+)+n(Na+)=n(Cl-)+2n(SO42-),据此计算SO42-的物质的量,离子数目之比等于二物质的量之比.
解答 解:设Na+、Fe3+、Cl-的物质的量分别为1mol、2mol、3mol,
根据电荷守恒可得:3n(Fe3+)+n(Na+)=n(Cl-)+2n(SO42-),
即:1mol+2×3mol=3mol+2n(SO42-),
解得:n(SO42-)=2mol,
物质的量之比等于离子数目之比,
则溶液中Fe3+和SO42-离子的个数比为2mol:2mol=1:1,
故选A.
点评 本题考查物质的量浓度的有关计算,侧重于学生的分析能力和计算能力的考查,题目难度中等,明确电荷守恒的含义为解答关键,注意掌握守恒思想在化学计算中的应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.大气中的SO2是造成酸雨的主要污染物.最新研究表明,离子晶体[N(CH3)4]2SO4(s) 能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂:
[N(CH3)4]2SO4(s)+SO2(g)?[N(CH3)4]2S2O6(s)
下列说法正确的是( )
[N(CH3)4]2SO4(s)+SO2(g)?[N(CH3)4]2S2O6(s)
下列说法正确的是( )
| A. | [N(CH3)4]+中只含共价键 | B. | 该反应中,SO2作氧化剂 | ||
| C. | SO2漂白品红是利用其强氧化性 |
18.下列化学符号中,数字“2”表示的意义不正确的是( )
| A. | 2Na:两个钠元素 | |
| B. | 2OH-:两个氢氧根离子 | |
| C. | $\stackrel{+2}{M}$g:镁元素的化合价为+2价 | |
| D. | NO2:一个二氧化氮分子含有两个氧原子 |
15. 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1一定温度下,在一个容积固定的密闭容器中,发生上述反应,下列不能判断该反应达到化学平衡状态的是d (填字母).
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2mol H-O键
c. v正(CO)=v逆(H2O) d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
①该反应的逆反应为吸 (填“吸”或“放”)热反应
②若实验3要达到与实验2中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是b=2a且a>l (用含a、b的数学式表示).
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:
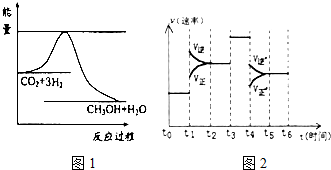
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)图1表示该反应进行过程中能量(单位为kJ?mol.)的变化.
①在体积为1L的恒容密闭容器中,充入l molCO2和3molH2,下列措施中能使 c (CH3OH)增大的是cd (填字母)
a.升高温度
b.充入He (g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入l mol CO2和3molH2
②当反应达到平衡时不断改变条件(但不改变各组分物质的量和状态)反应速率随时间的变化如图2:其中表示平衡混合物中CH3OH含量最高的一段时间是t0~t1;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,则K1大于K2(填“大于”、“等于”或“小于”).
 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1一定温度下,在一个容积固定的密闭容器中,发生上述反应,下列不能判断该反应达到化学平衡状态的是d (填字母).
a.容器中的压强不变 b.1mol H-H键断裂的同时断裂2mol H-O键
c. v正(CO)=v逆(H2O) d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 0.4 | 3 |
| 3 | 900 | a | b | c | d | t |
②若实验3要达到与实验2中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是b=2a且a>l (用含a、b的数学式表示).
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)图1表示该反应进行过程中能量(单位为kJ?mol.)的变化.
①在体积为1L的恒容密闭容器中,充入l molCO2和3molH2,下列措施中能使 c (CH3OH)增大的是cd (填字母)
a.升高温度
b.充入He (g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入l mol CO2和3molH2
②当反应达到平衡时不断改变条件(但不改变各组分物质的量和状态)反应速率随时间的变化如图2:其中表示平衡混合物中CH3OH含量最高的一段时间是t0~t1;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,则K1大于K2(填“大于”、“等于”或“小于”).
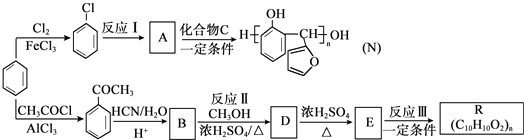

 .
. 生成
生成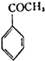 的反应类型是取代反应,D生成E的过程中,浓硫酸的作用催化剂和吸水剂.
的反应类型是取代反应,D生成E的过程中,浓硫酸的作用催化剂和吸水剂. .
.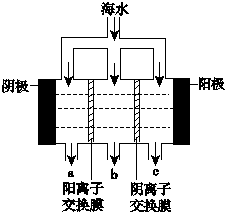 《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.
《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.