题目内容
20.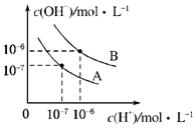 已知水在不同温度下的电离平衡曲线如图所示.(注:以下溶液混合时均不考虑体积的变化)
已知水在不同温度下的电离平衡曲线如图所示.(注:以下溶液混合时均不考虑体积的变化)(1)在曲线B 所对应的温度>25℃(填“>”、“<”或“=”),该温度下0.05mol•L-1Ba(OH)2 溶液的pH=11.
(2)25℃时,将pH=9 的NaOH 溶液与pH=4 的HCl 溶液混合,若所得混合
溶液的pH=7,则NaOH 溶液与HCl 溶液的体积之比为10:1.
(3)25℃时,若1L a mol•L-1 的某一元强酸溶液与1L b mol•L-1 的某一元
强碱溶液混合后溶液的pH=1,则a 与b 之间应满足的关系是a=b+0.2.
(4)25℃时,pH=2 的HCl 溶液和pH=11 的NH3•H2O 溶液中,若水的电离程度分别用α1、α2表示,则α1<α2(填“>”、“<”或“=”,下同);若二者恰好中和,则所得溶液的pH<7,其原因是NH4++H2O?NH3•H2O+OH-(用离子方程式表示).
分析 (1)图象中B点氢离子浓度和氢氧根离子浓度为10-6mol/L,温度一定存在离子积常数Kw=10-12,据此计算0.05mol•L-1Ba(OH)2 溶液的pH,A点为常温Kw=10-14;
(2)根据溶液的pH计算出溶液中氢离子、氢氧根离子浓度,再列式计算出氢氧化钠溶液和硫酸溶液的体积;
(3)25℃时,若1L a mol•L-1 的某一元强酸溶液与1L b mol•L-1 的某一元强碱溶液混合后溶液的pH=1,计算过量氢离子浓度为0.1mol/L,据此列式计算;
(4)酸碱抑制水的电离,氢离子或氢氧根离子浓度越大抑制程度越大,若二者恰好中和,则所得溶液为氯化铵溶液,铵根离子水解显酸性;
解答 解:(1)图象中B点氢离子浓度和氢氧根离子浓度为10-6mol/L,温度一定存在离子积常数Kw=10-12,A点为常温Kw=10-14,水电离过程为吸热过程,加热促进电离,离子积常数增大,所以在曲线B 所对应的温度>25°C,B点Kw=10-12,0.05mol•L-1Ba(OH)2 溶液中c(OH-)=0.05mol/L×2=0.1mol/L,则溶液中氢离子浓度c(H+)=$\frac{1{0}^{-12}}{0.1}$=10-11mol/L,溶液的pH=11,
故答案为:>;11;
(2)25℃时所得混合溶液的pH=7,溶液呈中性即酸碱恰好中和,即n(OH-)=n(H+),则V(NaOH)•10-5 mol•L-1=V(H2SO4)•10-4 mol•L-1,得V(NaOH):V(H2SO4)=10:1,故答案为:10:1;
(3)25℃时,若1L a mol•L-1 的某一元强酸溶液与1L b mol•L-1 的某一元强碱溶液混合后溶液的pH=1,则c(H+)=$\frac{1L×amol.L-1L×bmol/L}{2L}$=0.1mol/L,
得到a=b+0.2,
故答案为:a=b+0.2;
(4)25℃时,pH=2 的HCl 溶液中氢离子浓度10-2mol/L,pH=11 的NH3•H2O 溶液中氢氧根离子浓度10-3mol/L,氢氧根离子浓度小于盐酸溶液中氢离子浓度,抑制水的电离程度小,若水的电离程度分别用α1、α2表示则α1<α2,若二者恰好中和,所得溶液为氯化铵溶液,铵根离子水解显酸性,则所得溶液的pH<7,其原因用离子方程式表示为:NH4++H2O?NH3•H2O+OH-,
故答案为:<;NH4++H2O?NH3•H2O+OH-;
点评 本题考查了弱电解质电离平衡影响因素、酸碱反应后溶液酸碱性判断和溶液PH计算,盐类水解等,掌握基础是解题关键,题目难度中等.

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案| A. | 石油分馏 | B. | 煤的干馏 | C. | 海水制镁 | D. | 海带提碘 |
| A. | 合金一定是由两种或多种金属熔合而成的 | |
| B. | 日常生活中用到的五角硬币属于铜合金 | |
| C. | 铝合金的硬度比铝的大,熔点比铝的高 | |
| D. | 商代的司母戊鼎是由纯铜打造而成的 |
| A. | ①②③④ | B. | ②④ | C. | ①②③ | D. | ①③④ |
| A. | 在水中加入少量NaHCO3固体 | B. | 在水中滴入少量稀硫酸 | ||
| C. | 在水中加入少量氯化铝固体 | D. | 将水加热到100℃,测得pH=6 |
| A. | 等于0.9mol | B. | 等于0.45mol | ||
| C. | 大于0.45mol,小于0.9mol | D. | 小于0.45mol |
| A. | 0.1mol/LFeC13溶液中:A13+、NH4+、Cl-、SCN- | |
| B. | 使甲基橙变红色的溶液中:Mg2+、K+、SO42-、NO3- | |
| C. | $\frac{{K}_{W}}{c({H}^{+})}$=1×10-15mol/L的溶液中:Na+、Fe3+、I-、AlO2- | |
| D. | 水电离的c(H+)=1×10-13mol/L的溶液中:K+、Na+、CO32-、SO42- |

 ,由A生成F的反应类型是加聚反应.
,由A生成F的反应类型是加聚反应. CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.