��Ŀ����
����ʽΪC12H14O2��F�л���㷺�����㾫�ĵ������Ϊ�˺ϳɸ����ʣ�ijʵ���ҵĿƼ���Ա��������кϳ�·�ߣ�

�Իش��������⣺
��1��A�����ں˴Ź����������ܳ��� �ַ壮
��2��C���ʵĹ��������� ��
��3�������ϳ�·��������ȡ����Ӧ���� �����ţ���
��4��д����Ӧ�Ļ�ѧ����ʽ�� ��
��5��F�ж���ͬ���칹�壬��д�������������������нṹ��ʽ�������ڷ����廯����Һ�����F��ͬ�Ĺ����ţ��ڱ�����������ȡ�������ұ����ϵ�һ�ȴ���ֻ�����֣�������һ��ȡ����Ϊ-CH2COOCH3�� ��

�Իش��������⣺
��1��A�����ں˴Ź����������ܳ���
��2��C���ʵĹ���������
��3�������ϳ�·��������ȡ����Ӧ����
��4��д����Ӧ�Ļ�ѧ����ʽ��
��5��F�ж���ͬ���칹�壬��д�������������������нṹ��ʽ�������ڷ����廯����Һ�����F��ͬ�Ĺ����ţ��ڱ�����������ȡ�������ұ����ϵ�һ�ȴ���ֻ�����֣�������һ��ȡ����Ϊ-CH2COOCH3��
���㣺�л�����ƶ�
ר�⣺�л���Ļ�ѧ���ʼ��ƶ�
����������A����ˮ�ļӳɲ�����ж�AΪ ����Ӧ����±������ˮ�ⷴӦ��������BΪ
����Ӧ����±������ˮ�ⷴӦ��������BΪ ��B����������Ӧ�õ�CΪ
��B����������Ӧ�õ�CΪ ����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ
����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ ����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ
����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ ��E��D����������Ӧ����FΪ
��E��D����������Ӧ����FΪ ���ݴ˽��
���ݴ˽��
 ����Ӧ����±������ˮ�ⷴӦ��������BΪ
����Ӧ����±������ˮ�ⷴӦ��������BΪ ��B����������Ӧ�õ�CΪ
��B����������Ӧ�õ�CΪ ����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ
����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ ����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ
����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ ��E��D����������Ӧ����FΪ
��E��D����������Ӧ����FΪ ���ݴ˽��
���ݴ˽�����
�⣺����A����ˮ�ļӳɲ�����ж�AΪ ����Ӧ����±������ˮ�ⷴӦ��������BΪ
����Ӧ����±������ˮ�ⷴӦ��������BΪ ��B����������Ӧ�õ�CΪ
��B����������Ӧ�õ�CΪ ����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ
����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ ����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ
����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ ��E��D����������Ӧ����FΪ
��E��D����������Ӧ����FΪ ��
��
��1��AΪ ����4�ֻ�ѧ������ͬ����ԭ�ӣ��ں˴Ź����������ܳ���4�ַ壬�ʴ�Ϊ��4��
����4�ֻ�ѧ������ͬ����ԭ�ӣ��ں˴Ź����������ܳ���4�ַ壬�ʴ�Ϊ��4��
��2��CΪ �����еĹ��������ƣ��Ȼ����ǻ����ʴ�Ϊ���Ȼ����ǻ���
�����еĹ��������ƣ��Ȼ����ǻ����ʴ�Ϊ���Ȼ����ǻ���
��3�������ϳ�·���У���Ӧ���Ǽӳɷ�Ӧ����Ӧ����������Ӧ����Ӧ������ȥ��Ӧ����Ӧ�ڢݢ�����ȡ����Ӧ���ʴ�Ϊ���ڢݢޣ�
��4����Ӧ�Ļ�ѧ����ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��5��F�� ���ж���ͬ���칹�壬��������������ͬ���칹�壺�����ڷ����廯����Һ�����F��ͬ�Ĺ����ţ��ڱ�����������ȡ�������ұ����ϵ�һ�ȴ���ֻ�����֣�������һ��ȡ����Ϊ-CH2COOCH3��������������
���ж���ͬ���칹�壬��������������ͬ���칹�壺�����ڷ����廯����Һ�����F��ͬ�Ĺ����ţ��ڱ�����������ȡ�������ұ����ϵ�һ�ȴ���ֻ�����֣�������һ��ȡ����Ϊ-CH2COOCH3��������������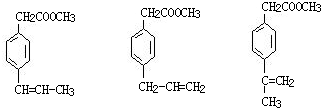 ��
��
�ʴ�Ϊ�� ��
��
 ����Ӧ����±������ˮ�ⷴӦ��������BΪ
����Ӧ����±������ˮ�ⷴӦ��������BΪ ��B����������Ӧ�õ�CΪ
��B����������Ӧ�õ�CΪ ����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ
����C��D�ķ���ʽ��֪��C������ȥ��Ӧ����D����D�����к���2��������DΪ ����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ
����Ӧ������±������ˮ�ⷴӦ����E�Ľṹ��ʽΪ ��E��D����������Ӧ����FΪ
��E��D����������Ӧ����FΪ ��
����1��AΪ
 ����4�ֻ�ѧ������ͬ����ԭ�ӣ��ں˴Ź����������ܳ���4�ַ壬�ʴ�Ϊ��4��
����4�ֻ�ѧ������ͬ����ԭ�ӣ��ں˴Ź����������ܳ���4�ַ壬�ʴ�Ϊ��4����2��CΪ
 �����еĹ��������ƣ��Ȼ����ǻ����ʴ�Ϊ���Ȼ����ǻ���
�����еĹ��������ƣ��Ȼ����ǻ����ʴ�Ϊ���Ȼ����ǻ�����3�������ϳ�·���У���Ӧ���Ǽӳɷ�Ӧ����Ӧ����������Ӧ����Ӧ������ȥ��Ӧ����Ӧ�ڢݢ�����ȡ����Ӧ���ʴ�Ϊ���ڢݢޣ�
��4����Ӧ�Ļ�ѧ����ʽΪ��
 ��
���ʴ�Ϊ��
 ��
����5��F��
 ���ж���ͬ���칹�壬��������������ͬ���칹�壺�����ڷ����廯����Һ�����F��ͬ�Ĺ����ţ��ڱ�����������ȡ�������ұ����ϵ�һ�ȴ���ֻ�����֣�������һ��ȡ����Ϊ-CH2COOCH3��������������
���ж���ͬ���칹�壬��������������ͬ���칹�壺�����ڷ����廯����Һ�����F��ͬ�Ĺ����ţ��ڱ�����������ȡ�������ұ����ϵ�һ�ȴ���ֻ�����֣�������һ��ȡ����Ϊ-CH2COOCH3�������������� ��
���ʴ�Ϊ��
 ��
��
���������⿼���л�����ƶϣ���Ŀ�Ѷ��еȣ�ע���������л���Ľṹ������ʽ��ȡ���������Ͻ����ƶϣ���Ҫѧ���������չ����ŵ������Լ������ŵ�ת����

��ϰ��ϵ�д�
 ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д� Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
�����Ŀ
ʵ������ת���ķ�Ӧ����ʽ�У���ȷ���ǣ�������
| A��H2SO3��H2SO4��2 H2SO3+O2=2 H2SO4 |
| B��Fe��Fe3+��2 Fe+6 H+=2 Fe3++3 H2�� |
| C��Br-��Br2��2 Br-+I2=Br2+2 I- |
| D��Cu��CuSO4��Cu+2 H2SO4��ϡ��=CuSO4+SO2��+2 H2O |
�����й����ʵ���;����������ǣ�������
| A�����������Ʊ�ľ�ķ������ԭ�� |
| B�������������������������������� |
| C���轺����ʵ���Һʹ�װʳƷ�ȵĸ���� |
| D��ʯӢ��ˮ������ʯ����Ҫ�ɷֶ��Ƕ������� |
3.2gͭ�����HNO3��8mol?L-1��30mL����ַ�Ӧ��HNO3�Ļ�ԭ����ΪNO2��NO����Ӧ����Һ������H+Ϊa mol����ԭ�����������������
| A��a mol |
| B����0.24-a��mol |
| C����0.1+a��mol |
| D����0.14-a��mol |
��һ����������ͨ��60mLŨ��Ϊ10.00mol/L���ȵ�����������Һ�У���Һ���γ�NaCl��NaClO��NaClO3������ϵ�������ж���ȷ���ǣ�������
| A����NaOH��Ӧ������һ��Ϊ0.3mol |
| B��n��Na+����n��Cl-������Ϊ7��3 |
| C������Ӧ��ת�Ƶĵ���Ϊnmol����0.3��n��0.5 |
| D��n��NaCl����n��NaClO����n��NaClO3������Ϊ11��2��1 |
 ijͬѧ���о�ǰ18��Ԫ��ʱ���֣����Խ������ų���ͼ��ʾ�ġ���ţ����״��ͼ��ÿ����?������һ��Ԫ�أ�����O�������Ԫ�أ�����˵���д�����ǣ�������
ijͬѧ���о�ǰ18��Ԫ��ʱ���֣����Խ������ų���ͼ��ʾ�ġ���ţ����״��ͼ��ÿ����?������һ��Ԫ�أ�����O�������Ԫ�أ�����˵���д�����ǣ�������| A����O��ԽԶ��Ԫ��ԭ�Ӱ뾶һ��Խ�� |
| B������������Ԫ�ش���ͬһ�壬AԪ��λ��Ԫ�����ڱ���A�� |
| C��BԪ����ͼ�н�������ǿ��Ԫ�� |
| D��B��C����������ˮ����������Ӧ |
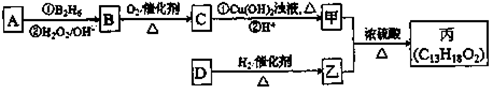
 ����Ϊͬϵ�������������������
����Ϊͬϵ�������������������