题目内容
天然碱的组成可以用aNa2CO3?bNaHCO3?cH2O(a、b、c为整数)表示.通过以下实验测定某天然碱的化学式,将质量为12.45g的某天然碱溶于水,逐滴滴加某浓度的稀盐酸,产生气体的体积与加入盐酸的体积(标准状况)的关系如下表所示:下列说法错误的是( )
| 盐酸体积(mL) | 20 | 40 | 60 | 80 |
| 产生气体体积(mL) | 0 | 560 | 1680 | 2520 |
| A、加入盐酸体积小于20 mL时,体系发生的离子反应为:CO32-+H+═HCO3- |
| B、加入盐酸体积为50 mL时,产生气体(标准状况)的体积为1120mL |
| C、本实验使用盐酸的浓度为2.5 mol?L-1 |
| D、该天然碱的化学式为Na2CO3?2NaHCO3?2H2O |
考点:化学方程式的有关计算
专题:
分析:A.加入20mL盐酸,不产生气体,说明发生反应:CO32-+H+═HCO3-;
B.加入80mL盐酸生成气体体积为2520mL,大于加入60mL盐酸时生成的气体体积,故加入40mL、60mL盐酸时,盐酸不足,完全反应,发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,加入50mL盐酸产生的气体体积为加入40mL盐酸产生的气体及在40mL基础上再加入10mL盐酸产生的气体体积之和,结合40mL~60mL之间消耗盐酸体积与生成气体体积的定比关系计算;40mL~60mL之间消耗20mL盐酸,生成气体1680mL-560mL=1120mL;
C.发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,根据盐酸和二氧化碳之间的关系式计算盐酸浓度;
D.发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,生成560mL二氧化碳消耗盐酸的体积=
×20mL=10mL,故加入前30mL盐酸,发生反应Na2CO3+HCl=NaCl+NaHCO3,30mL~75mL发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,由两阶段消耗的盐酸体积,可计算天然碱中Na2CO3、NaHCO3的物质的量之比,再根据生成二氧化碳计算各自物质的量,根据质量守恒计算结晶水的质量,进而计算结晶水的物质的量,确定三者比例关系,进而确定天然碱的化学式.
B.加入80mL盐酸生成气体体积为2520mL,大于加入60mL盐酸时生成的气体体积,故加入40mL、60mL盐酸时,盐酸不足,完全反应,发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,加入50mL盐酸产生的气体体积为加入40mL盐酸产生的气体及在40mL基础上再加入10mL盐酸产生的气体体积之和,结合40mL~60mL之间消耗盐酸体积与生成气体体积的定比关系计算;40mL~60mL之间消耗20mL盐酸,生成气体1680mL-560mL=1120mL;
C.发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,根据盐酸和二氧化碳之间的关系式计算盐酸浓度;
D.发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,生成560mL二氧化碳消耗盐酸的体积=
| 560mL |
| 1120mL |
解答:
解:A.加入20mL盐酸,不产生气体,说明发生反应:CO32-+H+═HCO3-,故A正确;
B.加入80mL盐酸生成气体体积为2520mL,大于加入60mL盐酸时生成的气体体积,故加入40mL、60mL盐酸时,盐酸不足,完全反应,发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,40mL~50mL之间消耗10mL盐酸,生成气体体积为(1680mL-560mL)×
=560mL,故加入50mL盐酸产生的气体体积为:560mL+560mL=1120mL,故B正确;
C.40mL~60mL之间消耗20mL盐酸,生成气体1680mL-560mL=1120mL,发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,设盐酸的浓度为c,
NaHCO3+HCl=NaCl+CO2↑+H2O
1 1
0.02cmol
1:1=0.02cmol:
c=2.5mol/L,故C正确;
D.发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,生成560mL二氧化碳消耗盐酸的体积=
×20mL=10mL,故加入前30mL盐酸,发生反应Na2CO3+HCl=NaCl+NaHCO3,从产生气体到生成2520mL二氧化碳消耗盐酸的体积=
×10mL=45mL,即完全生成气体共消耗盐酸30+45=75mL,30mL~75mL发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,
令天然碱中Na2CO3、NaHCO3的物质的量为amol、bmol,则:
Na2CO3+HCl=NaCl+NaHCO3,
amol amol amol
NaHCO3 +HCl=NaC l+CO2↑+H2O,
(a+b)mol (a+b)mol (a+b)mol
故amol:(a+b)mol=30mL:45mL,则a:b=2:1,由生成二氧化碳可知(a+b)mol=0.1125mol,解得a=0.075、b=0.0375,故天然碱中结晶水的质量=12.45g-0.0375mol×84g/mol-0.075mol×106g/mol=1.35g,结晶水的物质的量=
=0.075mol,
则天然碱中n(Na2CO3):n(NaHCO3):n(H2O)=0.075mol:0.0375mol:0.075mol=2:1:2,
故天然碱的化学式为:2Na2CO3?NaHCO3?2H2O,故D错误;
故选D.
B.加入80mL盐酸生成气体体积为2520mL,大于加入60mL盐酸时生成的气体体积,故加入40mL、60mL盐酸时,盐酸不足,完全反应,发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,40mL~50mL之间消耗10mL盐酸,生成气体体积为(1680mL-560mL)×
| (50-40)mL |
| (60-40)mL |
C.40mL~60mL之间消耗20mL盐酸,生成气体1680mL-560mL=1120mL,发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,设盐酸的浓度为c,
NaHCO3+HCl=NaCl+CO2↑+H2O
1 1
0.02cmol
| 1.12L |
| 22.4L/mol |
1:1=0.02cmol:
| 1.12L |
| 22.4L/mol |
c=2.5mol/L,故C正确;
D.发生反应:NaHCO3+HCl=NaCl+CO2↑+H2O,生成560mL二氧化碳消耗盐酸的体积=
| 560mL |
| 1120mL |
| 2520mL |
| 560mL |
令天然碱中Na2CO3、NaHCO3的物质的量为amol、bmol,则:
Na2CO3+HCl=NaCl+NaHCO3,
amol amol amol
NaHCO3 +HCl=NaC l+CO2↑+H2O,
(a+b)mol (a+b)mol (a+b)mol
故amol:(a+b)mol=30mL:45mL,则a:b=2:1,由生成二氧化碳可知(a+b)mol=0.1125mol,解得a=0.075、b=0.0375,故天然碱中结晶水的质量=12.45g-0.0375mol×84g/mol-0.075mol×106g/mol=1.35g,结晶水的物质的量=
| 1.35g |
| 18g/mol |
则天然碱中n(Na2CO3):n(NaHCO3):n(H2O)=0.075mol:0.0375mol:0.075mol=2:1:2,
故天然碱的化学式为:2Na2CO3?NaHCO3?2H2O,故D错误;
故选D.
点评:本题考查混合物计算、根据方程式计算,碳酸钠与盐酸的反应分两步进行,先找出完全反应点,再根据完全反应的点确定范围,综合考查学生各方面素质,难度很大,属于易错题目.

练习册系列答案
相关题目
分子式为C5H10O2属于羧酸的同分异构体数目有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
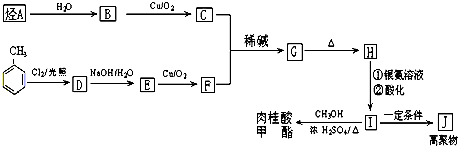
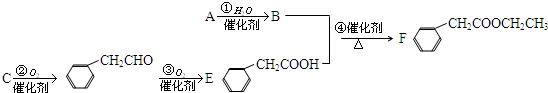
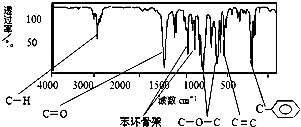 肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.
肉桂酸甲酯是调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精,用于肥皂、洗涤剂、风味剂和糕点的调味,在医药工业中作为有机合成的中间体.