题目内容
19.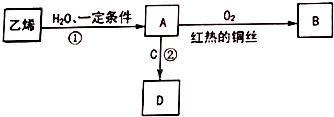 乙烯是一种重要的化工原料,可进行如图转化,其中C是食醋的主要成分.(部分反应物、生成物和反应条件已略去)
乙烯是一种重要的化工原料,可进行如图转化,其中C是食醋的主要成分.(部分反应物、生成物和反应条件已略去)请回答下列问题.
(1)反应①的化学方程式是CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3-CH2-OH.
(2)B的结构简式是CH3CHO,C中官能团的名称是羧基.
(3)反应②的化学方程式是CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O,反应类型是酯化反应,反应后可用饱和碳酸钠溶液除去D中混有的C.
CH3COOCH2CH3+H2O,反应类型是酯化反应,反应后可用饱和碳酸钠溶液除去D中混有的C.(4)鉴别乙烯和甲烷的方法是将气体分别通入酸性高锰酸钾溶液中,若观察到酸性高锰酸钾溶液褪色,则证明气体是乙烯.
分析 乙烯与水加成生成乙醇A,A为C2H5OH,乙醇催化氧化生成B为CH3CHO,C是食醋的主要成分,应为CH3COOH,乙酸与乙醇反应生成D,D为CH3COOC2H5,以此解答该题.
解答 解:乙烯与水加成生成乙醇A,A为C2H5OH,乙醇催化氧化生成B为CH3CHO,C是食醋的主要成分,应为CH3COOH,乙酸与乙醇反应生成D,D为CH3COOC2H5,
(1)乙烯和水在催化作用下发生加成反应生成乙醇,方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3-CH2-OH,故答案为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3-CH2-OH;
(2)B为CH3CHO,C为CH3COOH,含有的官能团为羧基,故答案为:CH3CHO;羧基;
(3)乙酸与乙醇反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O,该反应的类型为酯化反应;乙酸乙酯不溶于饱和碳酸钠溶液,而乙酸与碳酸钠反应,可用饱和碳酸钠溶液除杂,
CH3COOCH2CH3+H2O,该反应的类型为酯化反应;乙酸乙酯不溶于饱和碳酸钠溶液,而乙酸与碳酸钠反应,可用饱和碳酸钠溶液除杂,
故答案为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;酯化反应;饱和碳酸钠溶液;
CH3COOCH2CH3+H2O;酯化反应;饱和碳酸钠溶液;
(4)乙烯含有碳碳双键,可被酸性高锰酸钾氧化而使溶液褪色,鉴别乙烯和甲烷,可将气体分别通入酸性高锰酸钾溶液中,观察到酸性高锰酸钾溶液褪色的为乙烯,
故答案为:将气体分别通入酸性高锰酸钾溶液中;酸性高锰酸钾溶液褪色.
点评 本题考查有机推断,为高考常见题型和高频考点,涉及烯烃、醇、醛、羧酸等性质,是对有机化合物知识的综合考查,能较好的考查考生的思维能力,把握乙烯和水反应的特点以及乙醇的性质,难度不大.

练习册系列答案
相关题目
9.乙醇在发生催化氧化时,化学键断裂的位置是(如图)( )


| A. | ②③ | B. | ③④ | C. | ①③ | D. | ②④ |
7.实验室用蔗糖配制50.0g溶质的质量分数为10%的蔗糖溶液,下列说法错误的是( )
| A. | 用量程为10 mL的量筒量取所需的水 | |
| B. | 用托盘天平称取5.0 g蔗糖 | |
| C. | 溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒 | |
| D. | 将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签 |
14.下列反应在一定条件下,能达到化学平衡状态的是( )
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | 2SO2+O2$?_{△}^{催化剂}$2SO3 | ||
| C. | NaOH+HNO3═NaNO3+H2O | D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
4.下列物质属于非电解质的是( )
| A. | 稀硫酸 | B. | Cu | C. | SO2 | D. | NaOH |
11. 某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图所示),得到的实验数据如表所示:
某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图所示),得到的实验数据如表所示:
已知:西红柿、苹果果汁都是显酸性.
(1)该实验的目的是探究水果种类和电极间距离对水果电池电流大小的影响.
(2)能表明水果种类对电流大小有影响的实验编号是②和③.
(3)图所示的装置中,负极的电极反应式为Zn-2e-=Zn2+,正极附近区域c(H+)将减小(填“增大”、“减小”、“不变”),总反应离子方程式为Zn+2H+=Zn2++H2↑.
 某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图所示),得到的实验数据如表所示:
某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图所示),得到的实验数据如表所示:已知:西红柿、苹果果汁都是显酸性.
| 实验编号 | 水果种类 | 电极间距离/cm | 电流大小/?A |
| ① | 西红柿 | 1 | 98.7 |
| ② | 西红柿 | 2 | 72.5 |
| ③ | 苹果 | 2 | 27.2 |
(2)能表明水果种类对电流大小有影响的实验编号是②和③.
(3)图所示的装置中,负极的电极反应式为Zn-2e-=Zn2+,正极附近区域c(H+)将减小(填“增大”、“减小”、“不变”),总反应离子方程式为Zn+2H+=Zn2++H2↑.
8.下列关于金属冶炼的叙述正确的是( )
| A. | 工业上可利用铝热反应大量冶炼金属铁 | |
| B. | 金属钠、铝和铜都可用热还原法制备 | |
| C. | CO还原磁铁矿得到9 mol铁时转移24 mol电子 | |
| D. | 电解饱和氯化镁溶液可得金属镁 |
9.如图为铜锌原电池示意图,下列说法正确的是( )
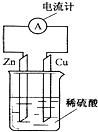

| A. | 锌片逐渐溶解 | B. | 电子由铜片通过导线流向锌片 | ||
| C. | 烧杯中溶液逐渐呈蓝色 | D. | 该装置能将电能转变为化学能 |