题目内容
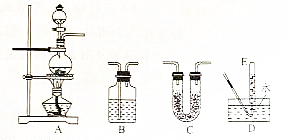
20.某化学兴趣小组利用如图装罝进行某些物质的制备和性质实验(图中部分夹持装置省略).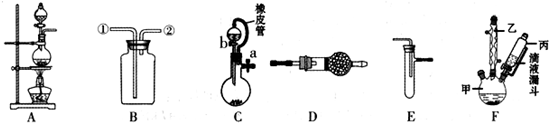
(1)为制取干燥氨气,可将装置C与D连接,C中橡皮管的作用是平衡分液漏斗与圆底烧瓶中压强,便于液体顺利流下;装置D中的固体宜选用碱石灰.
(2)利用装罝A和E组合实验可比较Cl2和I2的氧化性强弱.若E中盛有混合液体,下层是CCl4,充分反应后,振荡E,观察到能证明Cl2和I2氧化性强弱的实验现象是四氯化碳层由无色变为紫红色,其反应的离子方程式为Cl2+2I-=2Cl-+I2.
(3)在装罝B中装满水可用来收集NO,此时NO气体的入口是②(填①或②).
(4)利用装罝F可在实验室中制备对氯苯甲酸(
 ),有关反应、数据和实验步骤如下:
),有关反应、数据和实验步骤如下:
| 熔点/℃ | 沸点/℃ | 颜色 | 水溶性 | 相对分子质量 | |
| 对氯甲苯 | 7.5 | 162 | 无色 | 难溶 | 126.5 |
| 对氯苯甲酸 | 243 | 275 | 白色 | 微溶 | 156.5 |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐 | ||||
①量取6.OOmL对氯甲苯应选用的仪器是C(填正确选项的编号).
A.10mL量筒 B.50mL容量瓶 C.25mL酸式滴定管 D.25mL碱式滴定管
②控制温度在93℃左右的加热方法是水浴加热.
③将洗涤液与滤液合并后加入稀硫酸酸化时,可观察到的实验现象是产生白色沉淀.
④本实验的产率约为D(填正确选项的编号).
A.60% B.70% C.80% D.90%
分析 (1)平衡分液漏斗与圆底烧瓶中压强,便于液体顺利流下;D干燥氨气,可以盛放碱石灰;
(2)利用装罝A和E组合实验可比较Cl2和I2的氧化性强弱,A中制备氯气,E中发生置换反应生成碘单质;
(3)在装罝B中装满水可用来收集NO,从短管通入NO,从长导管排出水;
(4)①量取6.OOmL对氯甲苯,结合量取体积精度可知应选择滴定管,且对氯甲苯容易腐蚀橡皮管;
②控制温度在93℃左右,低于水的沸点,可以采取水浴加热;
③对氯苯甲酸钾属于可溶性盐,滤液、洗涤液中含有对氯苯甲酸钾,加入稀硫酸酸化时生成对氯苯甲酸;
④根据对氯甲苯质量计算对氯苯甲酸的理论产量,产率=$\frac{实际产量}{理论产量}$×100%.
解答 解:(1)C中橡皮管可以平衡分液漏斗与圆底烧瓶中压强,便于液体顺利流下;氨气为碱性气体,D干燥氨气,可以盛放碱石灰,
故答案为:平衡分液漏斗与圆底烧瓶中压强,便于液体顺利流下;碱石灰;
(2)利用装罝A和E组合实验可比较Cl2和I2的氧化性强弱,A中制备氯气,E中发生置换反应:Cl2+2I-=2Cl-+I2,生成碘单质,四氯化碳萃取溶液中的碘,静置分层,四氯化碳层由无色变为紫红色,
故答案为:四氯化碳层由无色变为紫红色;Cl2+2I-=2Cl-+I2;
(3)在装罝B中装满水可用来收集NO,从短管通入NO,从长导管排出水,
故答案为:②;
(4)①量取6.OOmL对氯甲苯,结合量取体积精度可知应选择滴定管,且对氯甲苯容易腐蚀橡皮管,应选择酸式滴定管,
故答案为:C;
②控制温度在93℃左右,低于水的沸点,可以采取水浴加热,受热均匀,便于控制温度,
故答案为:水浴加热;
③对氯苯甲酸钾属于可溶性盐,滤液、洗涤液中含有对氯苯甲酸钾,加入稀硫酸酸化时生成对氯苯甲酸,现象是:产生白色沉淀,
故答案为:产生白色沉淀;
④由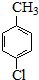 ~
~ ,可知对氯苯甲酸的理论产量为$\frac{6.42g}{126.5g/mol}$×156.5g,则对氯苯甲酸的产率为:[7.19g÷($\frac{6.42g}{126.5g/mol}$×156.5g)]×100%≈90.5%,
,可知对氯苯甲酸的理论产量为$\frac{6.42g}{126.5g/mol}$×156.5g,则对氯苯甲酸的产率为:[7.19g÷($\frac{6.42g}{126.5g/mol}$×156.5g)]×100%≈90.5%,
故选:D.
点评 本题考查有机物的制备实验、氨气的制备、气体收集、性质实验、实验基本操作等,属于拼合型题目,注意对题目信息的运用,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 10:7:11 | B. | 11:11:8 | C. | 11:10:8 | D. | 10:11:8 |
 某学生用0.10mol/L标准NaOH溶液滴定某浓度的盐酸,记录数据数据如下:
某学生用0.10mol/L标准NaOH溶液滴定某浓度的盐酸,记录数据数据如下:| 实验序号 | 待测液体积(ML) | 所消耗NaOH标准的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.50 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.4 |
(2)盐酸的物质的量浓度为0.10mol/L
(3)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是偏高(填“偏高”或“偏低”或“无影响”,下同).
(4)某同学用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,高锰酸钾溶液应盛放在甲中(填“甲”或“乙”),该反应的离子方程式为:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O.
(1)实验室用装置A制备C12的化学方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)①实验室在没有浓盐酸情况下,常用浓硫酸、食盐和二氧化锰在加热条件下制取氯气,则氧化剂与还原剂的质量之比为29:39.
②某研究性学习小组在查阅相关资料时发现二氧化锰与浓硫酸在加热条件下可产生O2和MnS04,其反应方程式为2Mn02+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$2MnSO4+O2↑+2H20.
③选用如图所示装置(装置可重复使用)和适当试剂,依次验证氯水的酸性、漂白性和氧化性,并证明制备C12时生成了O2.
供选试剂:MnO2、浓硫酸、食盐、饱和食盐水、紫色石蕊试液、酚酞试液、KBr溶液和CCl4的混合液、碱石灰、蒸馏水.将所用装置或仪器的序号按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称或化学式.
| 选用的仪器 | 加入的试剂 |
| A | 二氧化锰、浓硫酸、食盐 |
| B | 饱和食盐水 |
| B | KBr溶液和CCl4的混合液 |
| D |
⑤实验结束后,振荡盛有KBr溶液和CCl4的混合溶液的洗气瓶,现象为溶液分层,上层无色,下层为橙色.
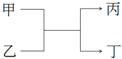 甲和丙为短周期、同主族元素组成的单质,乙和丁都是由两种元素组成的化合物,它们之间有如图所示的转化关系,则满足条件的甲和丙可能是下列各组物质中的( )
甲和丙为短周期、同主族元素组成的单质,乙和丁都是由两种元素组成的化合物,它们之间有如图所示的转化关系,则满足条件的甲和丙可能是下列各组物质中的( )| A. | H2和Na | B. | S和O2 | C. | C和Si | D. | Cl2和Br2 |
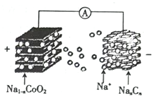 室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:
室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:NaCoO2+Cn$?_{放电}^{充电}$Na2-xCoO2+NaxCn
其电池结构如图所示.下列说法不正确的是( )
| A. | 充电时,Na+向正极移动 | |
| B. | 放电时,负极的电极反应式为NaxCn-xe-=xNa++Cn | |
| C. | 充电时,阴极质量减小 | |
| D. | 充电时,阳极的电极反应式为NaCoO2-xe-=Na1-xCoO2+xNa+ |