题目内容
15.下列状态的物质,既能导电又属于电解质的是( )| A. | 液态氯化氢 | B. | 浓硫酸 | C. | 熔融的KOH | D. | MgCl2晶体 |
分析 电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等.
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物等.
物质导电的条件:含有自由移动的电子和自由移动的离子.
解答 解:A.液态氯化氢,在水溶液中能导电的化合物,属于电解质,不含自由移动的电子和自由移动的离子,不导电,故A不选;
B.浓硫酸为混合物,不是电解质,故B不选;
C.熔融的KOH含有自由移动的离子,能够导电,是化合物,属于电解质,故C选;
D.氯化镁晶体在水溶液中或熔融状态下能导电的化合物,属于电解质,不含自由移动的电子和自由移动的离子,不导电,故D不选;
故选:C.
点评 本题考查了电解质、导电物质的判断,根据物质导电的实质及电解质定义来分析解答即可,难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
5.表是A、B、C、D五中有机物质的相关信息:
(1)A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(2)A与溴的四氯化碳溶液反应的生成物的结构简式CH2BrCH2Br;该生成物在一定条件下可用于制取最简单的二元醇方程式为:CH2BrCH2Br+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaBr.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在催化剂作用下,B与溴反应的化学方程式: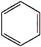 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.
(4)C与E反应能生成酯,该反应类型为取代反应;其化学反应方程式为:CH2=CHCOOH+CH3CH2OH$?_{△}^{H_{2}SO_{4}}$CH2=CHCOOOCH2CH3+H2O.
(5)D在一定条件下能发生银镜反应,其化学反应方程式:CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O.
| A | B | C | D | E |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为  | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯. | ①相对分子质量比C少2; ②能由C氧化而成; | ①由C、H、O三种元素组成; ②球棍模型为:  |
(2)A与溴的四氯化碳溶液反应的生成物的结构简式CH2BrCH2Br;该生成物在一定条件下可用于制取最简单的二元醇方程式为:CH2BrCH2Br+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaBr.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在催化剂作用下,B与溴反应的化学方程式:
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.(4)C与E反应能生成酯,该反应类型为取代反应;其化学反应方程式为:CH2=CHCOOH+CH3CH2OH$?_{△}^{H_{2}SO_{4}}$CH2=CHCOOOCH2CH3+H2O.
(5)D在一定条件下能发生银镜反应,其化学反应方程式:CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O.
6.下列说法中正确的是( )
| A. | 元素从化合态变为游离态,该元素一定被还原 | |
| B. | 铝合金比纯铝的熔点更高 | |
| C. | 保存FeCl3溶液时,通常在溶液中加少量的单质铁 | |
| D. | 漂白粉应隔绝空气密封保存 |
3.臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)?N2O5(g)+O2(g).若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是( )
| A | B | C | D |
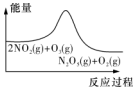 |  |  |  |
| 平衡后升温,NO2含量降低 | 0~2s内,v(O2)=0.2mol•L-1•s-1 | v正:b点>a点,b点:v逆>v正 | 恒温,t1时再充入O3 |
| A. | .A. | B. | .B | C. | .C | D. | .D |
10.下列有关说法正确的是( )
| A. | 标准状况下1molSO3的体积约为22.4L | |
| B. | pH小于7的雨水被称为酸雨 | |
| C. | 同温同压下,等质量的N2O4和NO2两种气体体积比为1:2 | |
| D. | 同温同压下,等质量的O2和SO2的所含原子个数比为1:1 |
20.下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A. | 碱性氧化物 氢氧化钙 Ca(OH)2 | B. | 酸性氧化物 二氧化碳 CO2 | ||
| C. | 酸 硫酸 H2S | D. | 盐 烧碱 Na2CO3 |
7.下列各组数据关系中,前者比后者大的是( )
| A. | 纯水100℃和25℃的pH值 | |
| B. | 氢硫酸溶液中的H+和HS-的浓度 | |
| C. | 100mL0.1mol/L的CH3COOH溶液与10mL1.0mol/L的CH3COOH溶液中H+数目 | |
| D. | 25℃,pH=11的KOH溶液与pH=3的CH3COOH溶液中由水电离出的OH-离子浓度 |
4.加热28.6g石碱晶体(Na2CO3 •10H2O )后得到12.4g固体残渣,则残渣的化学式是( )
| A. | Na2CO3 •H2O | B. | Na2CO3 •2H2O | C. | Na2CO3 | D. | 无法计算 |
17.下列离子的检验方法、现象及结论均合理的是( )
| A. | 向某溶液中先滴加氯水,再滴加KSCN溶滚,溶液显血红色,说明原溶液中含有Fe3+ | |
| B. | 向某溶液中滴加过量氨水,先有白色沉淀产生,然后沉淀溶解,说明原溶液中含有Al3+ | |
| C. | 向某溶液中滴加Ca(OH)2溶液,得到白色沉淀,说明原溶液中含有CO32- | |
| D. | 向某溶液中滴加过量NaOH溶液,得到蓝色沉淀,说明原溶液中含有Cu2+ |