题目内容
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
| B、遇苯酚显紫色的溶液:I-、K+、SCN-、Mg2+ |
| C、与铝反应产生大量氢气的溶液:NH4+、Na+、CO32-、NO3- |
| D、加入NaOH后加热既有气体放出又有沉淀生成的溶液:Ca2+、HCO3-、NH4+、CH3COO- |
考点:离子共存问题
专题:离子反应专题
分析:A.甲基橙呈红色的溶液为酸性溶液,溶液中存在大量的氢离子,偏铝酸根离子能够与氢离子反应;
B.遇苯酚显紫色的溶液中存在铁离子,铁离子与硫氰根离子反应生成硫氰化铁;
C.与铝反应生成氢气的溶液为酸性或者碱性溶液,铵根离子与氢氧根离子、碳酸根离子与氢离子反应;
D.加入氢氧化钠加热有气体,说明溶液中有铵根离子存在,有沉淀生成,钙离子、碳酸氢根离子与氢氧根离子反应生成碳酸钙沉淀.
B.遇苯酚显紫色的溶液中存在铁离子,铁离子与硫氰根离子反应生成硫氰化铁;
C.与铝反应生成氢气的溶液为酸性或者碱性溶液,铵根离子与氢氧根离子、碳酸根离子与氢离子反应;
D.加入氢氧化钠加热有气体,说明溶液中有铵根离子存在,有沉淀生成,钙离子、碳酸氢根离子与氢氧根离子反应生成碳酸钙沉淀.
解答:
解:A.该溶液中存在大量的氢离子,AlO2-与氢离子反应,在溶液中不能大量共存,故A错误;
B.该溶液中存在铁离子,SCN-与铁离子反应生成络合物硫氰化铁,在溶液中不能大量共存,故B错误;
C.该溶液为酸性或者碱性溶液,碱性溶液中,NH4+与氢氧根离子反应,酸性溶液中CO32-与氢离子反应,在溶液中不能大量共存,故C错误;
D.加入NaOH后加热既有气体放出又有沉淀生成,证明该溶液中存在铵根离子以及能跟OH-产生沉淀的金属阳离子,Ca2+、HCO3-、NH4+、CH3COO-离子之间不反应,且在溶液中能够大量共存,故D正确;
故选D.
B.该溶液中存在铁离子,SCN-与铁离子反应生成络合物硫氰化铁,在溶液中不能大量共存,故B错误;
C.该溶液为酸性或者碱性溶液,碱性溶液中,NH4+与氢氧根离子反应,酸性溶液中CO32-与氢离子反应,在溶液中不能大量共存,故C错误;
D.加入NaOH后加热既有气体放出又有沉淀生成,证明该溶液中存在铵根离子以及能跟OH-产生沉淀的金属阳离子,Ca2+、HCO3-、NH4+、CH3COO-离子之间不反应,且在溶液中能够大量共存,故D正确;
故选D.
点评:本题考查离子共存的正误判断,难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
ClO2是一种消毒杀菌效率高,二次污染小的水处理剂.实验室可通过以下反应制得:2NaClO3+Na2SO3+H2SO4═2ClO2+2Na2SO4+H2O,下列关于该反应的叙述正确的是( )
| A、NaClO3在反应中被氧化 |
| B、1mol NaClO3参加反应有2mol电子转移 |
| C、氧化性ClO2>NaClO3 |
| D、氧化产物与还原产物的物质的量之比为1:2 |
利用下列实验装置能完成相应实验的是( )

| A、图1装置制取少量乙酸乙酯 |
| B、图2装置制取并吸收HCl |
| C、图3装置量取8.5mL的稀硫酸 |
| D、图4装置模拟铁的腐蚀 |
 如图装置中发生反应的离子方程式为:Cu+2H+=Cu2++H2↑,下列说法正确的是( )
如图装置中发生反应的离子方程式为:Cu+2H+=Cu2++H2↑,下列说法正确的是( )| A、a、b不可能是同种材料的电极 |
| B、该装置可能是原电池,电解质溶液为稀盐酸 |
| C、该装置可能是a、b未形成闭合回路,电解质溶液是稀硝酸 |
| D、该装置可能是电解池,电解质溶液为稀盐酸 |
下列有机物中没有同分异构体的是( )
①邻二甲苯②二氯甲烷、丙烷④新戊烷⑤乙醇⑥乙酸⑦乙烯.
①邻二甲苯②二氯甲烷、丙烷④新戊烷⑤乙醇⑥乙酸⑦乙烯.
| A、①②③⑥ | B、②③⑤⑦ |
| C、②③⑦ | D、全部 |
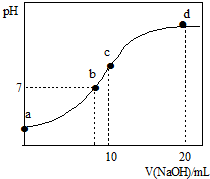 常温下,向20.00mL 0.1000mol?L-1(NH4)2SO4溶液中逐滴加入0.2000mol?L-1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发).下列说法正确的是( )
常温下,向20.00mL 0.1000mol?L-1(NH4)2SO4溶液中逐滴加入0.2000mol?L-1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发).下列说法正确的是( )| A、点a所示溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| B、点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C、点c所示溶液中:c(SO42-)+c(H+)=c(NH3?H2O )+c(OH-) |
| D、点d所示溶液中:c(SO42-)>c(NH3?H2O )>c(OH-)>c(NH4+) |
下列说法正确的是( )
A、用坩埚灼烧MgCl2?6H2O的化学反应方程式:MgCl2?6H2O
| ||||
| B、KSCN和FeCl3混合液存在着平衡:3KSCN+FeCl3?Fe(SCN)3+3KCl,加入少量KCl固体后溶液颜色不发生变化 | ||||
| C、常温下,将pH=2的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一 | ||||
D、 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,溶度积常数Ksp=c(Ba2+)?c(SO42-).则加入Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点 |
 将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物.
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物.