题目内容
15.以NA表示阿伏加德罗常数,下列说法中正确的是( )| A. | 3.2g的Cu与足量的浓HNO3反应生成的气体分子数为NA | |
| B. | pH=2的硫酸氢钠溶液中的硫酸根离子数为0.01NA | |
| C. | 8g CH4中含有的共价键总数为NA | |
| D. | 含有NA个中子的D2O的质量为2.0g |
分析 A、铜和浓硝酸反应后生成NO2气体,而NO2气体中存在平衡:2NO2?N2O4;
B、溶液体积不明确;
C、求出甲烷的物质的量,然后根据1mol甲烷中含4mol共价键来分析;
D、重水中含10个中子.
解答 解:A、铜和浓硝酸反应后生成NO2气体,而NO2气体中存在平衡:2NO2?N2O4,故3.2g铜反应后生成的气体分子个数小于NA个,故A错误;
B、溶液体积不明确,故溶液中的硫酸根的个数无法计算,故B错误;
C、8g甲烷的物质的量为0.5mol,而1mol甲烷中含4mol共价键,故0.5mol甲烷中含2NA条共价键,故C错误;
D、重水中含10个中子,故含NA个中子的重水的物质的量为0.1mol,则质量为2g,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
3.氯乙烯是合成高聚物聚氯乙烯的单体,工业制取氯乙烯需要以下反应:①乙炔与氯化氢反应生成氯乙烯 ②高温煅烧石灰石 ③电解饱和食盐水 ④制取乙炔 ⑤制取乙烯 ⑥合成氯化氢 ⑦制取水煤气 ⑧制取盐酸 ⑨制取电石,则制取氯乙烯的正确操作是( )
| A. | ③→⑧→①←④→⑨ | B. | ⑦→③→⑥→①←④→⑨→② | C. | ②→⑨→④→①←⑥←③ | D. | ②→④→⑤→①←⑥←③ |
7.某温度下.在一容积不变的密闭容器中充入2molSO2和1molO2,一段时间后反应达到平衡状态,测得平衡时的压强为反应前的0.8倍.则SO2的转化率为( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
4.下列化学用语中错误的是( )
| A. | 钠的原子结构示意图: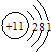 | B. | 甲烷的电子式: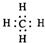 | ||
| C. | 异丁烷的结构简式: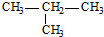 | D. | 偏铝酸钠的化学式:NaAlO2 |
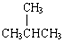 ;④CH4与C3H8;⑤CH3CH2CH2CH3与
;④CH4与C3H8;⑤CH3CH2CH2CH3与 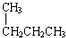 .请回答下列问题:
.请回答下列问题: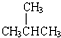 的名称是2-甲基丙烷.
的名称是2-甲基丙烷.
 .
. .
. 与过量的
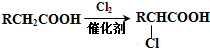
与过量的 也可以发生Reformatsky反应,试写出该生成物的结构简式
也可以发生Reformatsky反应,试写出该生成物的结构简式 .
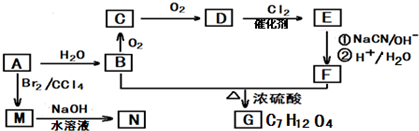
. (代号DMP)是一种常用的酯类塑化剂,其蒸汽对氢气的相对密度为97.工业上生产DMP的流程如图所示:
(代号DMP)是一种常用的酯类塑化剂,其蒸汽对氢气的相对密度为97.工业上生产DMP的流程如图所示:
 的名称1,2-二甲苯(或邻二甲苯),C中官能团的名称为醛基.
的名称1,2-二甲苯(或邻二甲苯),C中官能团的名称为醛基.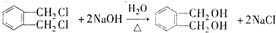 .
.
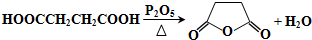
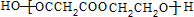 +(2n-1)H2O.
+(2n-1)H2O.