题目内容
下列除杂方法正确的是( )
| A、用金属钠除去乙醇中混有的少量水 |
| B、用酸性KmnO4溶液除去甲烷中混有的少量乙烯 |
| C、用H2除去乙烷中混有的少量乙烯 |
| D、用饱和Na2CO3溶液除去乙酸乙酯中混有的少量乙醇和乙酸 |
考点:物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.钠能与乙醇反应;
B.高锰酸钾具有强氧化性,能把乙烯氧化成二氧化碳;
C.氢气的量难以控制;
D.乙醇能溶于饱和Na2CO3溶液,乙酸能与饱和Na2CO3溶液反应生成乙酸钠、水、二氧化碳,乙酸乙酯不与饱和Na2CO3溶液反应.
B.高锰酸钾具有强氧化性,能把乙烯氧化成二氧化碳;
C.氢气的量难以控制;
D.乙醇能溶于饱和Na2CO3溶液,乙酸能与饱和Na2CO3溶液反应生成乙酸钠、水、二氧化碳,乙酸乙酯不与饱和Na2CO3溶液反应.
解答:
解:A.钠能与乙醇反应,将原物质除去,故A错误;
B.高锰酸钾具有强氧化性,能把乙烯氧化成二氧化碳,所以将混合气体通过酸性KMnO4溶液后除去乙烯但又产生二氧化碳,故B错误;
C.因H2与乙烯反应需要在催化剂、加热的条件下才能发生,常温下不反应,而且氢气的量难以控制,所以用H2不能除去乙烷中混有的少量乙烯,故C错误;
D.因乙醇能溶于饱和Na2CO3溶液,乙酸能与饱和Na2CO3溶液反应生成乙酸钠、水、二氧化碳,乙酸乙酯不与饱和Na2CO3溶液反应,也不溶于饱和Na2CO3溶液反应,出现分层现象,可用分液的方法分离,既除去了杂质,又没有引入新的杂质,符合除杂原则,故D正确.
故选D.
B.高锰酸钾具有强氧化性,能把乙烯氧化成二氧化碳,所以将混合气体通过酸性KMnO4溶液后除去乙烯但又产生二氧化碳,故B错误;
C.因H2与乙烯反应需要在催化剂、加热的条件下才能发生,常温下不反应,而且氢气的量难以控制,所以用H2不能除去乙烷中混有的少量乙烯,故C错误;
D.因乙醇能溶于饱和Na2CO3溶液,乙酸能与饱和Na2CO3溶液反应生成乙酸钠、水、二氧化碳,乙酸乙酯不与饱和Na2CO3溶液反应,也不溶于饱和Na2CO3溶液反应,出现分层现象,可用分液的方法分离,既除去了杂质,又没有引入新的杂质,符合除杂原则,故D正确.
故选D.
点评:本题考查物质的分离、提纯,侧重于学生的分析能力、实验能力和评价能力的考查,难度不大,注意把握物质的性质的异同,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
原子总数相同,各原子的外层电子数之和也相同的粒子,互称等电子体.等电子体的结构相似、物理性质相近.下列各组粒子不能互称为等电子体的是( )
| A、14CO和14N2 |
| B、O3和SO2 |
| C、CO2和N2O |
| D、N2H4和C2H4 |
水是最宝贵的资源之一.下列表述正确的是( )
A、H2O的电子式为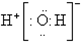 |
| B、4℃时,纯水的pH=7 |
| C、D216O中,质量数之和是质子数之和的两倍 |
| D、水分子在三种状态中,分子间的平均距离d:d(气态)>d(液态)>d(固态) |
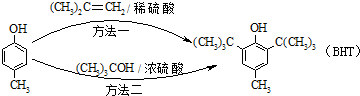
BHT(Butylated Hydroxy Toluene)是一种常用的食品抗氧化剂,合成方法有如下两种下列说法错误的是( )

A、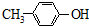 能与Na2CO3溶液反应 能与Na2CO3溶液反应 |
B、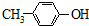 与BHT互为同系物 与BHT互为同系物 |
| C、BHT久置于空气中会被氧化 |
| D、两种方法的反应类型都是加成反应 |
下列关于硅及其化合物的说法正确的是( )
| A、自然界中存在大量硅单质 |
| B、硅酸盐广泛用于光纤通讯 |
| C、工艺师利用盐酸刻蚀石英制作艺术品 |
| D、高纯硅是应用广泛的半导体材料 |
一定量的锌粉和6mol/L的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,但不影响产生H2总量的是( )
①碳粉 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸 ⑥水.
①碳粉 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸 ⑥水.
| A、①③④ | B、①③⑤ |
| C、②④⑥ | D、③④⑤ |
NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、1 L 1 mol?L-1的氯化铁溶液中铁离子的数目为NA |
| B、标准状况下,2.24L CH2Cl2含有的分子数为0.1NA |
| C、78g Na2O2固体与足量H2O反应转移的电子数为NA |
| D、t℃时,1L pH=6的纯水中OH-的数目为10-8NA |
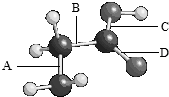 如图是氨基乙酸的球棍模型(图中的“棍”可能是单键,也可能是双键),该分子由四种元素的原子构成,它们原子半径的大小顺序是:X>Y>Z>W.
如图是氨基乙酸的球棍模型(图中的“棍”可能是单键,也可能是双键),该分子由四种元素的原子构成,它们原子半径的大小顺序是:X>Y>Z>W.