题目内容
将3.84g铜和一定量浓硝酸反应,随着反应的进行,硝酸的物质的量浓度降低,反应生成的气体颜色也变浅,当铜反应完毕后,共收集到标准状况下的气体2.24L.则
(1)反应方程式 ;
(2)生成硝酸铜的物质的量
(3)反应中被还原的硝酸的物质的量是
(4)反应中转移的电子数是 .
(1)反应方程式
(2)生成硝酸铜的物质的量
(3)反应中被还原的硝酸的物质的量是
(4)反应中转移的电子数是
考点:氧化还原反应的计算
专题:
分析:(1)随着反应的进行,硝酸的物质的量浓度降低,反应生成的气体颜色也变浅,发生Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(2)由于反应前后铜原子守恒,所以硝酸铜的物质的量即为铜的物质的量;
(3)反应后被还原的硝酸转化成气体NO或NO2,气体的物质的量即为被还原的硝酸的量;
(4)Cu失去电子,转移电子数等于Cu失去电子数.
(2)由于反应前后铜原子守恒,所以硝酸铜的物质的量即为铜的物质的量;
(3)反应后被还原的硝酸转化成气体NO或NO2,气体的物质的量即为被还原的硝酸的量;
(4)Cu失去电子,转移电子数等于Cu失去电子数.
解答:
解:(1)随着反应的进行,硝酸的物质的量浓度降低,反应生成的气体颜色也变浅,先发生Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O,后发生3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,故答案为:Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O;
(2)由Cu原子守恒可知,n(Cu(NO3)2)=n(Cu)=
=0.06 mol,故答案为:0.06mol;
(3)由反应Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O可知,气体的物质的量等于反应中被还原的硝酸的物质的量,
由N原子守恒可知,n(还原的硝酸)=n(气体)=
=0.1mol,故答案为:0.1mol;
(4)Cu失去电子,转移电子数等于Cu失去电子数,则转移电子为0.06mol×(2-0)×NA=0.12NA,故答案为:0.12NA.
(2)由Cu原子守恒可知,n(Cu(NO3)2)=n(Cu)=
| 3.84g |
| 64g/mol |
(3)由反应Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O可知,气体的物质的量等于反应中被还原的硝酸的物质的量,
由N原子守恒可知,n(还原的硝酸)=n(气体)=
| 2.24L |
| 22.4L/mol |
(4)Cu失去电子,转移电子数等于Cu失去电子数,则转移电子为0.06mol×(2-0)×NA=0.12NA,故答案为:0.12NA.
点评:本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析、计算及应用能力的考查,注意电子守恒、原子守恒的应用,题目难度不大.

练习册系列答案
相关题目
下列化学用语或模型表示正确的是( )
A、氯化氢的电子式: |
B、甲烷的球棍模型: |
C、 名称为2-甲基-2-戊烯 名称为2-甲基-2-戊烯 |
D、三硝基甲苯的结构简式: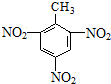 |
常温下,在amol?L-1的醋酸溶液中,以下说法不正确的是( )
| A、pH<7 |
| B、c(H+)>c(CH3COO-)>c(OH-) |
| C、c(CH3COO-)+c(CH3COOH)=amol?L-1 |
| D、c(H+)+c(CH3COOH)=c(CH3COO-)+c(OH-) |
下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A、铁生锈 |
| B、粗盐表面潮解 |
| C、浓硫酸的质量增大 |
| D、浓盐酸有白雾产生 |
下列关于化学键的说法正确的是( )
| A、构成单质分子的微粒一定含有共价键 |
| B、由非金属元素组成的化合物不一定是共价化合物 |
| C、非极性键只存在于双原子分子中 |
| D、不同元素组成的多原子分子里的化学键一定是极性键 |
 恒容体系,发生如下反应2A(g)?B(g)+xC(g)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图.某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度).
恒容体系,发生如下反应2A(g)?B(g)+xC(g)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图.某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度).