题目内容
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l、+2.已知Cu2O与稀硫酸反应,溶液呈蓝色.现向Cu、Cu2O和CuO组成的混合物中,加入1L 0.6mol/L HNO3溶液恰好使混合物溶解,同时收集到2240mL NO气体(标准状况).请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式 .
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 .
(3)若混合物中含0.1mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 .
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为 .
(1)写出Cu2O跟稀硝酸反应的离子方程式
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为
(3)若混合物中含0.1mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为
考点:化学方程式的有关计算,铜金属及其重要化合物的主要性质,有关混合物反应的计算
专题:计算题
分析:(1)硝酸具有强氧化性,Cu2O被稀HNO3氧化为Cu2+,NO3-被还原为NO,同时生成H2O,据此配平写出反应离子方程式;
(2)Cu、Cu2O、CuO与0.6mol HNO3恰好完全反应时生成Cu(NO3)2、NO和H2O,根据N原子守恒计算n[Cu(NO3)2],根据Cu元素守恒计算还原后得到Cu的物质的量,再根据m=nM计算固体Cu的质量;
(3)由Cu元素守恒可得:2n(Cu2O)+n(CuO)+n(Cu)=混合物中Cu原子物质的量,根据电子守恒可知:2n(Cu)+2n(Cu2O)=3n(NO),联立方程计算Cu2O、CuO的物质的量,Cu2O、CuO中氧原子与H2SO4反应结合H+生成H2O,据此计算消耗硫酸;
(4)根据电子守恒和铜原子守恒用n表示出n(Cu2O)、n(CuO).
(2)Cu、Cu2O、CuO与0.6mol HNO3恰好完全反应时生成Cu(NO3)2、NO和H2O,根据N原子守恒计算n[Cu(NO3)2],根据Cu元素守恒计算还原后得到Cu的物质的量,再根据m=nM计算固体Cu的质量;
(3)由Cu元素守恒可得:2n(Cu2O)+n(CuO)+n(Cu)=混合物中Cu原子物质的量,根据电子守恒可知:2n(Cu)+2n(Cu2O)=3n(NO),联立方程计算Cu2O、CuO的物质的量,Cu2O、CuO中氧原子与H2SO4反应结合H+生成H2O,据此计算消耗硫酸;
(4)根据电子守恒和铜原子守恒用n表示出n(Cu2O)、n(CuO).
解答:
解:(1)Cu2O被稀HNO3氧化为Cu2+,NO3-被还原为NO,同时生成H2O,其反应的离子方程式为:3Cu2O+14H++2NO3-═6Cu2++2NO↑+7H2O,
故答案为:3Cu2O+14H++2NO3-═6Cu2++2NO↑+7H2O;
(2)Cu、Cu2O、CuO与HNO3恰好完全反应时生成Cu(NO3)2、NO和H2O,硝酸的物质的量1L×0.6mol/L=0.6mol,NO的物质的量=
=0.1mol,根据N原子守恒可知:n[Cu(NO3)2]=
=0.25mol,混合物中所含的Cu元素共有0.25mol,根据铜元素守恒可知,用H2还原Cu、Cu2O、CuO混合物后应得到0.25mol Cu,故固体的质量为0.25mol×64g/mol=16g,
故答案为:16g;
(3)由Cu元素守恒可得:2×n(Cu2O)+n(CuO)+0.1mol=0.25mol,
由氧化还原反应得失电子守恒可知:0.1×2+2×n(Cu2O)=0.1mol×3,
解之得:n(Cu2O)=0.05mol,n(CuO)=0.05mol,
混合物中,0.1mol Cu不与稀H2SO4反应,0.05molCu2O、0.05molCuO与稀H2SO4反应,根据Cu2O、CuO中氧原子与H2SO4反应结合H+生成H2O,可得n(H2SO4)=0.05mol+0.05mol=0.1mol,
故答案为:0.1mol;
(4))由Cu元素守恒可得:2×n(Cu2O)+n(CuO)+n=0.25mol,
由氧化还原反应得失电子守恒可知:n×2+2×n(Cu2O)=0.1mol×3,
解之得:n(CuO)=n-0.05mol,
n(Cu2O)=0.15mol-n,
所以0.05mol<n<0.15mol.
故答案为:0.05mol<n<0.15mol.
故答案为:3Cu2O+14H++2NO3-═6Cu2++2NO↑+7H2O;
(2)Cu、Cu2O、CuO与HNO3恰好完全反应时生成Cu(NO3)2、NO和H2O,硝酸的物质的量1L×0.6mol/L=0.6mol,NO的物质的量=
| 2.24L |
| 22.4L/mol |
| 0.6mol-0.1mol |
| 2 |
故答案为:16g;
(3)由Cu元素守恒可得:2×n(Cu2O)+n(CuO)+0.1mol=0.25mol,
由氧化还原反应得失电子守恒可知:0.1×2+2×n(Cu2O)=0.1mol×3,
解之得:n(Cu2O)=0.05mol,n(CuO)=0.05mol,
混合物中,0.1mol Cu不与稀H2SO4反应,0.05molCu2O、0.05molCuO与稀H2SO4反应,根据Cu2O、CuO中氧原子与H2SO4反应结合H+生成H2O,可得n(H2SO4)=0.05mol+0.05mol=0.1mol,
故答案为:0.1mol;
(4))由Cu元素守恒可得:2×n(Cu2O)+n(CuO)+n=0.25mol,
由氧化还原反应得失电子守恒可知:n×2+2×n(Cu2O)=0.1mol×3,
解之得:n(CuO)=n-0.05mol,
n(Cu2O)=0.15mol-n,
所以0.05mol<n<0.15mol.
故答案为:0.05mol<n<0.15mol.
点评:本题考查混合物的计算,题目具有一定难度,侧重对学生思维能力的考查,(2)中注意根据守恒思想进行计算,(3)中利用反应生成水,根据H、O原子关系计算,避免利用方程式的繁琐.

练习册系列答案
相关题目
质量分数为15%的硫酸溶液18mL,密度为1.102g/mL,则它的物质的量的浓度最接近下列数值中的( )
| A、1.685mol/L |
| B、3.370mol/L |
| C、11.24mol/L |
| D、22.49mol/L |
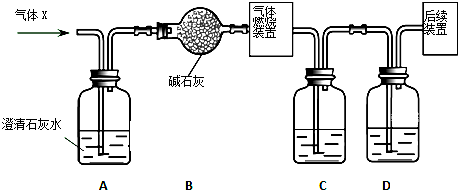
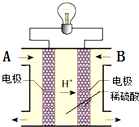 为解决环境、能源等问题,科学家正研究将CO2转化为CH3OH技术. 该转化反应为CO2+3H2=CH3OH+H2O.
为解决环境、能源等问题,科学家正研究将CO2转化为CH3OH技术. 该转化反应为CO2+3H2=CH3OH+H2O.