题目内容
实验室需要220mL0.1mol/L的碳酸钠溶液,现选取250ml容量瓶进行配制,以下操作正确的是( )
| A、用电子天平称7.15gNa2CO3?10H2O,配制成250ml溶液 |
| B、用电子天平称6.292gNa2CO3?10H2O,配制成250ml溶液 |
| C、用电子天平称2.65gNa2CO3,加入250mL水 |
| D、用电子天平称2.332g碳酸钠,配制成250mL溶液 |
考点:溶液的配制
专题:实验题
分析:需要220mL0.1mol/L的碳酸钠溶液,应选择250ml容量瓶,0.25L×0.1mol/L=0.025mol,需要碳酸钠的质量=0.025mol×106g/mol=2.65g;如果用Na2CO3?10H2O配置需要Na2CO3?10H2O的质量为0.025mol×286g/mol=7.15g,注意溶液的体积为250ml.
解答:
解:A.7.15gNa2CO3?10H2O中含有碳酸钠的物质的量为0.025mol,配制成250ml溶液,其物质的量浓度为0.1mol/L,故A正确;
B.6.292gNa2CO3?10H2O中含有碳酸钠的物质的量小于0.025mol,配制成250ml溶液,其物质的量浓度小于0.1mol/L,故B错误;
C.2.65.0gNa2CO3中含有碳酸钠的物质的量为0.025mol,加入250mL水,则溶液的体积大于250ml,其物质的量浓度小于0.1mol/L,故C错误;
D.2.332g碳酸钠中含有碳酸钠的物质的量小于0.025mol,配制成250ml溶液,其物质的量浓度小于0.1mol/L,故D错误;
故选:A.
B.6.292gNa2CO3?10H2O中含有碳酸钠的物质的量小于0.025mol,配制成250ml溶液,其物质的量浓度小于0.1mol/L,故B错误;
C.2.65.0gNa2CO3中含有碳酸钠的物质的量为0.025mol,加入250mL水,则溶液的体积大于250ml,其物质的量浓度小于0.1mol/L,故C错误;
D.2.332g碳酸钠中含有碳酸钠的物质的量小于0.025mol,配制成250ml溶液,其物质的量浓度小于0.1mol/L,故D错误;
故选:A.
点评:本题考查一定物质的量浓度溶液的配制,明确物质的量浓度的涵义是解题关键,注意溶液的体积与溶剂的体积的不同.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、2.4 g Mg与足量的盐酸反应失去的电子数为0.2NA |
| B、1 mol?L-1的氨水中含有NH3?H2O的分子数为NA |
| C、11.2L NH3所含有的分子数为0.5 NA |
| D、标准状况下NA 个SO3分子所占有的体积约为22.4L |
有关下列两种溶液的说法中,正确的是( )①0.1mol?L-1 CH3COONa溶液 ②0.1mol?L-1 CH3COOH溶液.
| A、相同温度下,溶液中水的电离程度:溶液①>溶液② | ||
| B、等体积混合溶液①和溶液②,所得溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | ||
C、加水稀释溶液①,溶液中
| ||
D、向溶液①中加少量的CH3COONa固体则
|
减少酸雨产生的途径可采取下列中的哪些措施:①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等⑤开发新能源( )
| A、①②③ | B、②③④⑤ |
| C、①③⑤ | D、①③④⑤ |
FeS2在空气中充分燃烧的化学方程式为4FeS2+11O2
2Fe2O3+8SO2,若ag FeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为( )
| ||
A、
| ||
B、
| ||
C、
| ||
D、
|
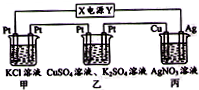
 如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,设A池中原混合液的体积为200mL.
如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,设A池中原混合液的体积为200mL.