题目内容
11.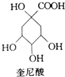 奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图所示,下列有关奎尼酸的说法中错误的是( )
奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图所示,下列有关奎尼酸的说法中错误的是( )| A. | 分子式为C7H12O6 | B. | 不能发生加成反应 | ||
| C. | 能与乙醇发生酯化反应 | D. | 1mol奎尼酸最多能消耗6molNaOH |
分析 由结构可知分子式,分子中含-COOH、-OH,结合羧酸、醇的性质来解答.
解答 解:A.奎尼酸的分子式是C7H12O6,故A正确;
B.不含不饱和键,不能发生加成反应,故B正确;
C.含有羧基,可发生酯化反应,故C正确;
D.只有羧基与氢氧化钠溶液反应,则1mol奎尼酸最多能消耗1molNaOH,故D错误.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重羧酸、醇的性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
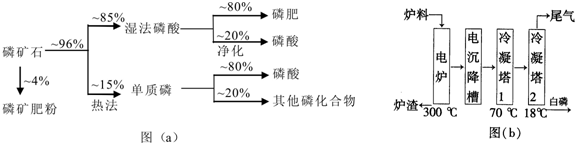
19.磷矿石主要以磷酸钙〔Ca3(PO4)2•H2O〕和磷灰石[Ca5F(PO4)3Ca5(OH)(PO4)3]等形式存在.图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸.图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程.
部分物质的相关性质如表:
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的69%.
(2)以磷灰石为原料,湿法磷酸过程中Ca3F(PO4)3反应的化学方程式为:Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑.现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85%的商品磷酸0.49 吨.
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷.炉渣的主要成分是:CaSiO3(填化学式),冷凝塔1的主要沉积物是:液态白磷,冷凝塔2的主要沉积物是:固态白磷.
(4)尾气中主要含有SiF4、CO,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去SiF4、H2S、HF
再通入次氯酸钠溶液,可除去PH3(均填化学式).
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是:产品纯度高.

部分物质的相关性质如表:
| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水,具有还原性 |
| SiF4 | -90 | -86 | 易水解 |
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的69%.
(2)以磷灰石为原料,湿法磷酸过程中Ca3F(PO4)3反应的化学方程式为:Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑.现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85%的商品磷酸0.49 吨.
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷.炉渣的主要成分是:CaSiO3(填化学式),冷凝塔1的主要沉积物是:液态白磷,冷凝塔2的主要沉积物是:固态白磷.
(4)尾气中主要含有SiF4、CO,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去SiF4、H2S、HF
再通入次氯酸钠溶液,可除去PH3(均填化学式).
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是:产品纯度高.
6.根据下列实验现象所得出的结论不正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机层呈橙色 | 氧化性:Cl2>KBrO3 |
| B | 向KNO3和KOH混合溶液中加入铝粉并加热,将湿润的红色石蕊试纸放在试管口 | 试纸变为蓝色 | NO3-被还原为NH3 |
| C | 向0.1mol•L-1的Na2CO3溶液中加入两滴酚酞,溶液显浅红色,微热. | 红色加深 | 盐类水解是吸热反应 |
| D | 将0.1mol•L-1的MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1的CuSO4溶液 | 白色沉淀逐渐变为蓝色沉淀 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| A. | A | B. | B | C. | C | D. | D |
3.在有机物分子中,若碳原子连接四个不同的原子或原子团,该碳原子称为不对称碳原子(或手性碳原子).具有手性碳原子的有机物具有光学活性.下列分子中,含有两个手性碳原子的是( )
| A. | 乳酸 CH3-CHOH-COOH | |
| B. | 甘油 CH2OH-CHOH-CH2OH | |
| C. | 脱氧核糖 CH2OH-CHOH-CHOH-CH2-CHO | |
| D. | 核糖 CH2OH-CHOH-CHOH-CHOH-CHO |
20.LiAlH4在125℃分解为LiH、H2和Al.下列说法中不正确的是( )
| A. | 乙醛在LiAlH4的作用下生成乙醇,LiAlH4作还原剂 | |
| B. | LiH中两种微粒半径:H->Li+ | |
| C. | 1mol LiAlH4在125℃完全分解,则转移4mol电子 | |
| D. | LiH溶于水的化学反应方程式:LiH+H2O═LiOH+H2↑ |
1.下列说法不正确的是( )
| A. | 常温下,向醋酸钠溶液中滴加盐酸至溶液呈中性一定有:c(CH3COOH)=c(Cl-) | |
| B. | NaHSO4溶液中滴加Ba(OH)2至溶液恰好呈中性c(Na+)>c(SO42-)>c(OH-)=c(H+) | |
| C. | 某酸式盐NaHA溶液中一定有:c(OH-)+c(A2-)=c(H+)+c(H2A) | |
| D. | 0.5 mol/L 的Na2S溶液中:$\frac{1}{2}$ c(Na+)=c(H2S)+c(HS-)+c(S2-)=0.5 mol/L |


 .
.