题目内容
(1)2.5mol Ba(OH)2中含有 个Ba2+,含有 个OH-,2.5mol Ba(OH)2的质量是 g.
(2)0.3mol NH3分子中所含原子数与 个H2O分子中所含原子数相等.
(3)含有0.4mol Al3+的Al2(SO4)3溶液中所含SO
的物质的量是 .(以上各题用数字填空.)
(2)0.3mol NH3分子中所含原子数与
(3)含有0.4mol Al3+的Al2(SO4)3溶液中所含SO
2- 4 |
考点:物质的量的相关计算
专题:化学实验与化学计算
分析:(1)根据物质的构成,氢氧化钡为强电解质,1mol氢氧化钡电离出1mol钡离子和2mol氢氧根离子,结合N=nNA、m=nM解答;
(2)依据微粒数之比等于物质的量之比,结合N=nNA计算;
(3)1mol硫酸铝电离产生3mol硫酸根离子、2mol铝离子.
(2)依据微粒数之比等于物质的量之比,结合N=nNA计算;
(3)1mol硫酸铝电离产生3mol硫酸根离子、2mol铝离子.
解答:
解:(1)由化学式可知,2.5mol Ba(OH)2中含有2.5mol Ba2+,5molOH-,由N=nNA可知Ba2+个数为2NA,即1.505×1024,OH-个数为5NA,即3.01×1024,2.5mol Ba(OH)2的质量m=n×M=2.5mol×171g/mol=427.5g,
故答案为:1.505×1024;3.01×1024;427.5;
(2)0.3mol NH3中所含氢原子物质的量为0.9mol;氢原子数之比等于物质的量之比,H2O分子中所含原子数也为0.9mol,需水0.45mol,由N=nNA可知H2O分子个数为0.45×6.02×1023=2.408×1023,
故答案为:2.408×1023;
(3)硫酸铝的电离方程为:Al2(SO4)3=2Al3++3SO42-,1mol硫酸铝电离产生3mol硫酸根离子、2mol铝离子两者之比为2:3,所以含有0.4mol Al3+的Al2(SO4)3溶液中所含SO42-:0.4×
mol=0.6mol,
故答案为:0.6 mol.
故答案为:1.505×1024;3.01×1024;427.5;
(2)0.3mol NH3中所含氢原子物质的量为0.9mol;氢原子数之比等于物质的量之比,H2O分子中所含原子数也为0.9mol,需水0.45mol,由N=nNA可知H2O分子个数为0.45×6.02×1023=2.408×1023,
故答案为:2.408×1023;
(3)硫酸铝的电离方程为:Al2(SO4)3=2Al3++3SO42-,1mol硫酸铝电离产生3mol硫酸根离子、2mol铝离子两者之比为2:3,所以含有0.4mol Al3+的Al2(SO4)3溶液中所含SO42-:0.4×
| 3 |
| 2 |
故答案为:0.6 mol.
点评:本题考查物质的量的有关计算,明确物质的构成为解答的关键,把握物质的量、微粒数目的关系即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列结构式表示一种有机物的结构: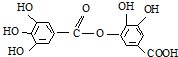 关于它的性质叙述中,正确的是( )
关于它的性质叙述中,正确的是( )
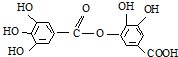 关于它的性质叙述中,正确的是( )
关于它的性质叙述中,正确的是( )| A、它有弱酸性,能与KOH反应 |
| B、可以水解生成一种生成物 |
| C、不能与强碱溶液反应 |
| D、可以水解生成两种生成物 |
 某种甲酸酯水解反应方程式为:
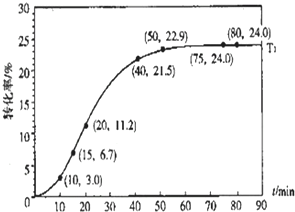
某种甲酸酯水解反应方程式为: 工业生产中用CO可以合成甲醇CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.
工业生产中用CO可以合成甲醇CO(g)+2H2(g)?CH3OH(g),△H=-90.1kJ?mol-1在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示.