题目内容
17.(1)将1.0mol CH4和2.0mol H2O ( g )通入容积固定为10L的反应容器中,在一定条件下发生反应:CH4 ( g )+H2O ( g )?CO ( g )+3H2 ( g ),测得在一定的压强下CH4的转化率与温度的关系如图1.
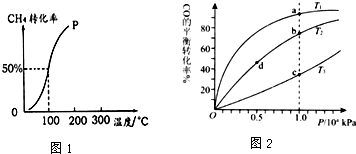
①该反应的△H>0(填“>”“<”或“=”)
②假设100℃时达到平衡所需的时间为3min,则用H2表示该反应的平均反应速率为0.05mol/(L•min).
③100℃时该反应的平衡常数的数值为0.0225.
④可用来判断该反应达到平衡状态的标志有AEF(填字母).
A.CO的含量保持不变 B.CH4浓度与CO浓度相等
C.ν正(CH4)=3ν逆(H2) D.混合气体的密度保持不变
E.混合气体的总物质的量保持不变 F.混合气体的压强度保持不变
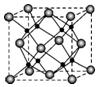
(2)生成甲醇的反应:CO (g)+2H2 (g)?CH3OH (g)△H=-129.0kJ/mol,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图2所示.下列说法正确的是CD(填字母).
A.温度:T1>T2>T3
B.正反应速率:ν(a)>ν(c); ν(b)>ν(d)
C.平衡常数:K(a)>K(c); K(b)=K(d)
D.平均摩尔质量:M(a)>M(c); M(b)>M(d)
(3)工业上利用甲醇制备氢气的常用方法之一为:甲醇蒸气重整法.该法中的一个主要反应为CH3OH(g)?CO(g)+2H2(g),此反应能自发进行的原因是该反应是一个熵增的反应..
分析 (1)①由图可知,温度越高,转化率越大;
②100℃时达到平衡所需的时间为3min,甲烷转化率为50%,则生成氢气为1.5mol,结合v=$\frac{△c}{△t}$计算;
③CH4 ( g )+H2O ( g )?CO ( g )+3H2 ( g )
开始 0.1 0.2 0 0
转化 0.05 0.05 0.05 0.15
平衡 0.05 0.15 0.05 0.15
结合平衡浓度计算K;
④结合平衡的特征“等、定”及衍生的物理量判定;
(2)A.该反应为放热反应,温度越低,转化率越低;
B.a、c温度不同,b、d压强不同,温度越大压强越大,反应速率越快;
C.K只与温度有关,温度越高,放热反应的K越小;
D.质量不变,CO的转化率越大,平衡后气体的物质的量越小,则M越大;
(3)由CH3OH(g)?CO(g)+2H2(g)可知,△H>0,△S>0,以此来解答.
解答 解:(1)①由图可知,温度越高,转化率越大,则升高温度平衡正向移动,该反应的△H>0,故答案为:>;
②100℃时达到平衡所需的时间为3min,甲烷转化率为50%,则生成氢气为1.5mol,用H2表示该反应的平均反应速率为$\frac{\frac{1.5mol}{10L}}{3min}$=0.05mol/(L•min),
故答案为:0.05;
③CH4 ( g )+H2O ( g )?CO ( g )+3H2 ( g )
开始 0.1 0.2 0 0
转化 0.05 0.05 0.05 0.15
平衡 0.05 0.15 0.05 0.15
K=$\frac{0.05×0.1{5}^{3}}{0.05×0.15}$=0.0225,
故答案为:0.0225;
④A.CO的含量保持不变,为平衡状态,故A选;
B.CH4浓度与CO浓度相等,与转化率、起始量有关,不能判断平衡状态,故B不选;
C.ν正(CH4)=3ν逆(H2),正逆反应速率不等,故C不选;
D.混合气体的密度始终保持不变,不能判定平衡状态,故D不选;
E.该反应为气体物质的量不等的反应,混合气体的总物质的量保持不变,为平衡状态,故E选;
F.该反应为气体物质的量不等的反应,混合气体的压强度保持不变,为平衡状态,故F选;
故答案为:AE;
(2)A.该反应为放热反应,温度越低,转化率越低,则温度:T2>T2>T1,故A错误;
B.a、c温度不同,b、d压强不同,温度越大压强越大,反应速率越快,则正反应速率:ν(a)<ν(c)、ν(b)>ν(d),故B错误;
C.K只与温度有关,温度越高,放热反应的K越小,则平衡常数:K(a)>K(c)、K(b)=K(d),故C正确;
D.质量不变,CO的转化率越大,平衡后气体的物质的量越小,则M越大,则平均摩尔质量:M(a)>M(c)、M(b)>M(d),故D正确;
故答案为:CD;
(3)由CH3OH(g)?CO(g)+2H2(g)可知,△H>0,△S>0,△H-T△S<0的反应可自发进行,则此反应能自发进行的原因是该反应是一个熵增的反应 (△S>0),故答案为:该反应是一个熵增的反应.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、平衡移动,反应进行方向为解答的关键,侧重分析与计算能力的考查,注意图象与平衡移动的结合,题目难度不大.

| A. | K不变,平衡可能移动 | B. | 平衡移动,K值一定变化 | ||
| C. | 平衡移动,K值可能不变 | D. | K值变化,平衡一定移动 |

(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:
CH4(g)+H2O(g)?CO(g)+3H2(g)…Ⅰ.CH4的转化率与温度、压强的关系如图1.
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为0.0030 mol/(L•min).
②图中的P1<P2(填“<”、“>”或“=”),100℃时平衡常数为2.25×10-4.
③该反应的△H>0(填“<”、“>”或“=”).
(2)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)?CH3OH(g);△H<0…Ⅱ.
①若容器容积不变,下列措施可增加甲醇产率的是BD.
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
| 实验编号 | T(℃) | n(CO)/n(H2) | p(MPa) |
| 1 | 150 | $\frac{1}{3}$ | 0.1 |
| 2 | a | $\frac{1}{3}$ | 5 |
| 3 | 350 | b | 5 |
B.根据反应Ⅱ的特点,图2是在压强分别为0.1MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强Px=0.1MPa.
| 温度℃ | 450 | 500 | 550 | 600 |
| SO2的转化率% | 97.5 | 95.8 | 90.50 | 80.0 |
(2)能判断该反应是否达到平衡状态的是ACF
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO3的浓度不变 D.C(SO2)=C(SO3)
E.V正(SO2)=V正(SO3) F.V正(SO3)=2V逆(O2)
(3)某温度下经2min反应达到平衡后C(SO2)=0.08mol•L-1.
①0~2min之间,O2的反应速率为0.08mol•L-1•min-1.
②此时的温度为600℃.
③此温度下的平衡常数为$\frac{400}{21}$(可用分数表示).
(4)若将平衡反应混合物的压强增大(假如体积可变),平衡将正向移动.
| A. | MgO | B. | HClO | C. | Cu2O | D. | ClO2 |

 M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题: