题目内容
(1)有等体积、等pH的Ba(OH)2和NH3?H2O两种溶液,用等浓度的盐酸来滴定,恰好中和时,用去酸的体积分别为V1、V2,则有:V1 V2(填“>”、“<”或“=”)
(2)常温下,等体积、等pH的醋酸和硫酸溶液中:c(CH3COO-) c(SO42-)(填“>”、“<”或“=”)
(3)在AgCl悬浊液中加入过量KI溶液,白色沉淀转化为黄色沉淀.加入过量KI溶液充分反应后,溶液中Ksp(AgCl) (填“增大”、“减小”或“不变”)
(4)在0.10mol?L-1 氨水中,加入少量NH4Cl晶体后,则 NH3?H2O的电离程度 (填“增大”、“减小”或“不变”)
(2)常温下,等体积、等pH的醋酸和硫酸溶液中:c(CH3COO-)
(3)在AgCl悬浊液中加入过量KI溶液,白色沉淀转化为黄色沉淀.加入过量KI溶液充分反应后,溶液中Ksp(AgCl)
(4)在0.10mol?L-1 氨水中,加入少量NH4Cl晶体后,则 NH3?H2O的电离程度
考点:酸碱混合时的定性判断及有关ph的计算,弱电解质在水溶液中的电离平衡,pH的简单计算,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)等pH时,氨水为弱碱、氢氧化钡为强碱,则氨水的浓度大于氢氧化钡,等体积的两溶液中,氨水的物质的量大于氢氧化钡,则氨水消耗的盐酸体积大于氢氧化钡;
(2)pH相同,则醋酸和硫酸溶液中氢离子浓度相等,根据电荷守恒判断c(CH3COO-)、c(SO42-)的关系;
(3)难溶物的溶度积与温度有关,温度不变,则溶度积不变;
(4)氨水中存在电离平衡,加入氯化铵后溶液中铵根离子浓度增大,抑制了氨水的电离.
(2)pH相同,则醋酸和硫酸溶液中氢离子浓度相等,根据电荷守恒判断c(CH3COO-)、c(SO42-)的关系;
(3)难溶物的溶度积与温度有关,温度不变,则溶度积不变;
(4)氨水中存在电离平衡,加入氯化铵后溶液中铵根离子浓度增大,抑制了氨水的电离.
解答:
解:(1)等体积、等pH的Ba(OH)2和NH3?H2O两种溶液,由于氨水为弱碱,一水合氨在溶液中部分电离,则氨水的浓度大于氢氧化钡,用等浓度的盐酸来滴定,恰好中和时,用去酸的体积分别为V1、V2,则氨水消耗的盐酸体积大于氢氧化钡,即:V1<V2,
故答案为:<;
(2)常温下,等体积、等pH的醋酸和硫酸溶液中,两溶液中氢离子浓度一定相同,根据电荷守恒可知:c(CH3COO-)=2c(SO42-),则c(CH3COO-)>c(SO42-),
故答案为:>;
(3)氯化银的溶度积Ksp(AgCl)与温度有关,与离子的浓度大小无关,由于温度不变,则氯化银的溶度积Ksp(AgCl)不变,
故答案为:不变;
(4)在0.10mol?L-1 氨水中存在电离平衡:NH3.H2O?NH4++OH-,加入少量NH4Cl晶体后,溶液中铵根离子浓度增大,抑制了氨水的电离,则 NH3?H2O的电离程度减小,
故答案为:减小.
故答案为:<;
(2)常温下,等体积、等pH的醋酸和硫酸溶液中,两溶液中氢离子浓度一定相同,根据电荷守恒可知:c(CH3COO-)=2c(SO42-),则c(CH3COO-)>c(SO42-),
故答案为:>;
(3)氯化银的溶度积Ksp(AgCl)与温度有关,与离子的浓度大小无关,由于温度不变,则氯化银的溶度积Ksp(AgCl)不变,
故答案为:不变;
(4)在0.10mol?L-1 氨水中存在电离平衡:NH3.H2O?NH4++OH-,加入少量NH4Cl晶体后,溶液中铵根离子浓度增大,抑制了氨水的电离,则 NH3?H2O的电离程度减小,
故答案为:减小.
点评:本题考查了酸碱混合的定性判断及溶液pH的计算、弱电解质的电离及其影响、难溶物的溶解平衡及其影响因素等知识,题目难度中等,注意掌握溶液酸碱性与溶液pH的计算方法,明确影响难溶物溶度积的因素.

练习册系列答案
相关题目
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标况下,22.4 L水中含有NA个H2O分子 |
| B、14 g N2含有的核外电子总数为NA |
| C、1 mol乙烯中含2 NA个碳碳双键 |
| D、2.3 g金属钠与足量水反应时失去的电子数是0.1NA |
下列有关叙述正确的是( )
| A、氢键是一种特殊化学键,它广泛地存在于自然界中 |
B、在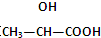 分子中含有1个手性C原子 分子中含有1个手性C原子 |
| C、碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子 |
| D、含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |

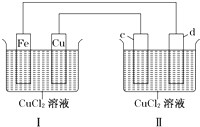 下列装置可实现电解CuCl2溶液,c、d均为石墨.读图回答下列问题:
下列装置可实现电解CuCl2溶液,c、d均为石墨.读图回答下列问题: 和
和

 ⅢA族的硼、铝、镓、铟、铊等元素和ⅤA族的氮、磷、砷、锑、铋等元素形成的化合物在研究和生产中有许多重要用途.请回答下列问题.
ⅢA族的硼、铝、镓、铟、铊等元素和ⅤA族的氮、磷、砷、锑、铋等元素形成的化合物在研究和生产中有许多重要用途.请回答下列问题.