题目内容
15.下表是元素周期表的一部分,请回答有关问题:| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)④元素与⑦元素形成的化合物的电子式
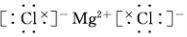 .
.(3)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4.(填化学式)
分析 由元素在周期表的位置可知,①~⑩分别C、N、F、Mg、Al、S、Cl、Ar、K、Br,
(1)氢氧化铝为两性,Al与KOH反应生成偏铝酸钾和水;
(2)④元素与⑦元素形成的化合物为氯化镁;
(3)高氯酸为所有含氧酸中酸性最强的酸.
解答 解:由元素在周期表的位置可知,①~⑩分别C、N、F、Mg、Al、S、Cl、Ar、K、Br,
(1)氢氧化铝为两性,则表中能形成两性氢氧化物的元素是Al,该元素的单质与⑨最高价氧化物的水化物反应的化学方程式为2Al+2KOH+2H2O=2KAlO2+3H2↑,
故答案为:Al;2Al+2KOH+2H2O=2KAlO2+3H2↑;
(2)④元素与⑦元素形成的化合物为氯化镁,其电子式为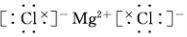 ,故答案为:
,故答案为: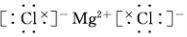 ;
;
(3)高氯酸为所有含氧酸中酸性最强的酸,则①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4,故答案为:HClO4.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、元素的性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
12.晶体结构属于面心结构的是( )
| A. | NaCl | B. | CsCl | C. | CO2 | D. | Cu |
6.已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是( )

| A. | 由红外光谱可知,该有机物中至少有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机分子中有三种不同化学环境的氢原子 | |
| C. | 仅由A的核磁共振氢谱可以得知其分子中的氢原子总数 | |
| D. | 若A的化学式为C2H6O,则其结构简式为CH3CH2OH |
3.常温下能用来盛放浓硝酸的金属器皿是( )
| A. | Na | B. | Mg | C. | Al | D. | Cu |
10. 合成氨工业对国民经济和社会发展具有重的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa 下,n(NH3)和 n(H2)随时间 t 变 化的关系示意图如图所示.下列叙述中正确的是( )
合成氨工业对国民经济和社会发展具有重的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa 下,n(NH3)和 n(H2)随时间 t 变 化的关系示意图如图所示.下列叙述中正确的是( )
 合成氨工业对国民经济和社会发展具有重的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa 下,n(NH3)和 n(H2)随时间 t 变 化的关系示意图如图所示.下列叙述中正确的是( )
合成氨工业对国民经济和社会发展具有重的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa 下,n(NH3)和 n(H2)随时间 t 变 化的关系示意图如图所示.下列叙述中正确的是( )| A. | c 点处正反应速率和逆反应速率相等 | |
| B. | a 点处正反应速率比 b 点处的大 | |
| C. | d 点(t1 时刻)和 e 点(t2 时刻)处 n(N2)不同 | |
| D. | t2 时刻,正反应速率大于逆反应速率 |
20.反应A+B=C+D的能量变化如图所示,下列说法正确的是( )


| A. | 该反应为放热反应 | B. | 该反应吸收的能量为(E1-E2) | ||
| C. | 反应物A的能量低于生成物C的能量 | D. | 该反应只有在加热条件下才能进行 |
7.除去物质中所含少量杂质(括号内为杂质),所选用试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性高锰酸钾 | 洗气 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 溴苯(液溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
4.常温下pH=2的盐酸溶液和pH=12的NaOH溶液,下列叙述中不正确的是( )
| A. | 两溶液中水的电离程度相同 | |
| B. | 盐酸溶液中c(Cl-)等于NaOH溶液中c (Na+) | |
| C. | 若两溶液等体积混合能恰好中和 | |
| D. | 分别稀释10倍后,两溶液的pH之和大于14 |
