题目内容
9.下列电子式书写不正确的是( )| A. | 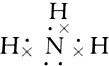 | B. | 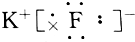 | C. | 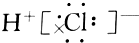 | D. | 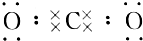 |
分析 A.N原子的最外层有5个电子,其中3个未成对电子和1对成对电子;
B.钾离子与氟离子通过离子键结合;
C.氯化氢属于共价化合物;
D.CO2是共价化合物,碳原子有四个电子分别和氧原子形成两对共用电子对.
解答 解:A.N原子的最外层有5个电子,其中3个未成对电子和1对成对电子,3个未成对电子分别和3个H原子形成3对共用电子对,电子式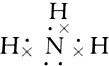 ,故A正确;
,故A正确;
B.氟化钾为离子化合物,钾离子与氟离子通过离子键结合,电子式为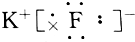 ,故B正确;
,故B正确;
C.氯化氢为共价化合物,氢原子与氯原子共用1对电子,电子式为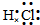 ,故C错误;
,故C错误;
D.CO2是共价化合物,碳原子有四个电子分别和氧原子形成两对共用电子对,电子式为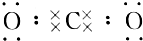 ,故D正确.
,故D正确.
故选C.
点评 本题考查电子式的正误判断,题目难度不大,该题是基础性试题的考查,也是高考中的常见题型,主要是考查学生对常见物质电子式的熟悉了解程度,明确物质中化学键的类型是解题的关键.

练习册系列答案
相关题目
20.下列叙述正确的是( )
| A. | 浓硫酸有氧化性,稀硫酸没有氧化性 | |
| B. | 稀释浓硫酸时,将浓硫酸沿着量筒壁慢慢注入盛水的量筒中,并不断搅拌 | |
| C. | 硝酸浓度越大氧化能力越强 | |
| D. | 金属和硝酸反应,浓度由浓到稀,对应的还原产物有NO2、NO和H2 |
4.分子式为C10H14的芳香烃中,苯环上一溴代物有两种结构的物质共有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
14.下列说法正确的是( )
| A. | 加热法可以除去氯化铵中的少量碘单质 | |
| B. | 向试液中滴加双氧水可KSCN溶液,溶液变为红色,则试液中一定含Fe2+ | |
| C. | 向某固体中滴加稀硫酸,产生的气体能使澄清石灰水变浑浊,则该固体一定是苏打或小苏打 | |
| D. | 向含少量硫酸铁的硫酸铜溶液中加入过量的氧化铜,过滤,得到纯净硫酸铜溶液 |
 高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是其它化学知识的载体.
高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是其它化学知识的载体. 钛(Ti)被称为继铁、铝之后的第三金属.
钛(Ti)被称为继铁、铝之后的第三金属.