题目内容
19.将含有0.400mol CuSO4和0.200mol FeCl3水溶液1L,用惰性电极电解一段时间后在电极上析出19.2g Cu,此时在另一电极上放出的气体在标状况下的体积为( )| A. | 5.60L | B. | 6.72L | C. | 4.48L | D. | 7.84L |
分析 用惰性电极电解混合溶液时,阴极反应式依次是Fe3++e-=Fe2+、Cu2++2e-=Cu、2H++2e-=H2↑,阳极反应式依次是2Cl--2e-=Cl2↑、4OH--4e-=2H2O+O2↑,
当阳极上析出19.2gCu时,析出n(Cu)=$\frac{19.2g}{64g/mol}$=0.3mol<0.4mol,说明铜离子没有完全放电,阴极上铁离子得电子生成亚铁离子,所以阴极转移电子物质的量=n(Fe3+)+2n(Cu)=0.2mol+2×0.3mol=0.8mol;
阳极上氯离子先放电,氯离子完全放电时转移电子物质的量=n(Cl-)=0.2mol×3=0.6mol<0.8mol,所以还有0.2mol电子是氢氧根离子放电转移的,则生成氧气物质的量=$\frac{0.2mol}{4}$=0.05mol,根据V=nVm计算生成气体体积.
解答 解:用惰性电极电解混合溶液时,阴极反应式依次是Fe3++e-=Fe2+、Cu2++2e-=Cu、2H++2e-=H2↑,阳极反应式依次是2Cl--2e-=Cl2↑、4OH--4e-=2H2O+O2↑,
当阳极上析出19.2gCu时,析出n(Cu)=$\frac{19.2g}{64g/mol}$=0.3mol<0.4mol,说明铜离子没有完全放电,阴极上铁离子得电子生成亚铁离子,所以阴极转移电子物质的量=n(Fe3+)+2n(Cu)=0.2mol+2×0.3mol=0.8mol;
阳极上氯离子先放电,氯离子完全放电时转移电子物质的量=n(Cl-)=0.2mol×3=0.6mol<0.8mol,所以还有0.2mol电子是氢氧根离子放电转移的,则生成氧气物质的量=$\frac{0.2mol}{4}$=0.05mol,
根据Cl原子守恒得生成n(Cl2)=$\frac{1}{2}$n(Cl-)=$\frac{1}{2}$×0.6mol=0.3mol,
所以生成气体在标况下体积=(0.05+0.3)mol×22.4L/mol=7.84L,故选D.
点评 本题考查电解原理,为高频考点,明确离子放电顺序是解本题关键,根据离子放电顺序及转移电子守恒进行计算,注意阴极上铁离子先得电子,为易错点.

 阅读快车系列答案
阅读快车系列答案| A. | H2O2是氧化剂,H2O2中的氧元素被还原 | |
| B. | 每生成1 mol O2转移的电子的物质的量为2 mol | |
| C. | ClO2中的氯元素被氧化 | |
| D. | ClO2是氧化剂,H2O2是还原剂 |
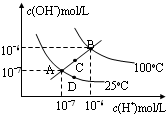
| A. | 图中四点Kw间的关系:A=D<C<B | |
| B. | 若从A点到D点,可采用:温度不变在水中加少量酸 | |
| C. | 若从A点到C点,可采用:温度不变在水中加少量NaAc固体 | |
| D. | 若从A点到D,可采用:温度不变在水中加少量NaAc固体 |
| A. | H+、Ba2+、Cl-、NO3- | B. | K+、AlO2-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO3- | D. | Fe3+、NH4+、SCN-、Cl- |
| A. | 常温常压下,22.4L氮气所含原子数目大于2NA | |
| B. | 1 mol Na2O2跟H2O反应转移的电子数目为2NA | |
| C. | 标准状态下,22.4L三氧化硫所含分子数目大于NA | |
| D. | 1 mol甲烷的质量与0.5 mol O2的质量不相等 |
| A. | 称量错误 | |
| B. | H2O2分解不完全 | |
| C. | Na2O2转化为Na0H和H2O2的反应不完全 | |
| D. | 装置漏气 |
| A. |  表示0.001 mol•L一1盐酸滴定0.001 mol•L一1NaOH溶液的滴定曲线 | |
| B. | 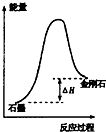 所示,石墨的熔点比金刚石低 | |
| C. | 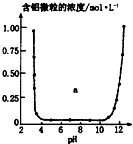 表示的是Al3+与OH一反应时含铝微粒浓度变化曲线,图中a区域的物质是Al(OH)3 | |
| D. | 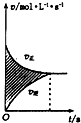 所示,图中的阴影部分面积的含义是[v(正)-v(逆))] |