题目内容
19.几种物质在酸性溶液中的还原性强弱顺序如下:SO2>I->Fe2+>H2O2.据此判断下列反应不能发生的是( )| A. | 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ | B. | H2O2+H2SO4=SO2↑+O2↑+2H2O | ||
| C. | SO2+I2+2H2O=H2SO4+2HI | D. | 2Fe3++2I-=2Fe2++I2 |
分析 根据氧化还原反应中还原剂的还原性大于还原产物的还原性,利用酸性溶液中还原性强弱的顺序是SO2>I->Fe2+>>H2O2来判断反应能否发生.
解答 解:A.因该反应中S元素的化合价升高,Fe元素的化合价降低,则SO2为还原剂,还原性强弱为SO2>Fe2+,与已知的还原性强弱一致,能发生,故A不选;
B.因该反应中O元素的化合价升高,S元素的化合价降低,则H2O2为还原剂,还原性强弱为H2O2>SO2,与已知的还原性强弱不一致,不能发生,故B选;
C.因该反应中S元素的化合价升高,I元素的化合价降低,则SO2为还原剂,还原性强弱为SO2>HI,与已知的还原性强弱一致,反应能发生,故C不选;
D.因该反应中Fe元素的化合价降低,I元素的化合价升高,则I-为还原剂,还原性强弱为I->Fe2+,与已知的还原性强弱一致,能发生,故D不选.
故选B.
点评 本题考查利用已知的还原性强弱来判断化学反应的发生,学生应学会利用化合价来分析反应中的还原剂,并利用还原剂的还原性大于还原产物的还原性来解答即可,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.下列有关物质检验的操作、现象及结论均正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水中,变石灰水浑浊 | 该溶液中一定含有CO32- |
| C | 向无色溶液中滴加氯水,再加CCl4振荡、静置、溶液分层,下层呈紫红色 | 该溶液中一定含有I- |
| D | 取洁净的铂丝在酒精灯火焰上灼烧至无色,再蘸取少量溶液置于火焰上灼烧,火焰呈黄色,通过蓝色钴玻璃观察,火焰呈紫色 | 该溶液一定含有Na+、K+ |
| A. | A | B. | B | C. | C | D. | D |
10.CO2的摩尔质量为( )
| A. | 44g | B. | 44g/mol | C. | 44 | D. | 22.4L/mol |
10.等物质的量的下列化合物与足量浓盐酸反应,得到氯气的物质的量最多的是( )
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |
7.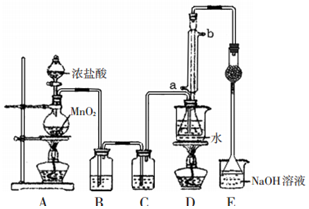 S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
已知:S2Cl2易与水反应.
下列是几种物质的熔沸点.
(1)写出装置A中制备Cl2的化学反应方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)装置B中盛放试剂的作用是吸收Cl2中的HCl气体; 装置C中的试剂是浓硫酸.
(3)D装置中采用水浴加热的优点是受热均匀,温度易控制; 反应结束后,从D装置锥形瓶内的混合物中分离出产物S2Cl2的实验方法是蒸馏.
(4)装置E中倒扣漏斗的作用是防止倒吸.
(5)S2Cl2易与水反应,有淡黄色沉淀生成,产生的无色气体能使品红溶液褪色,写出该反应的化学方程式2S2Cl2+2H2O=3S↓+SO2↑+4HCl.
 S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).
S2Cl2是工业上常用的硫化剂,实验室利用反应:CS2+3Cl2=CCl4+S2Cl2来制备S2Cl2,反应装置如图所示(部分夹持装置省略).已知:S2Cl2易与水反应.
下列是几种物质的熔沸点.
| 物质 | 沸点/℃ | 熔点/℃ |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(2)装置B中盛放试剂的作用是吸收Cl2中的HCl气体; 装置C中的试剂是浓硫酸.
(3)D装置中采用水浴加热的优点是受热均匀,温度易控制; 反应结束后,从D装置锥形瓶内的混合物中分离出产物S2Cl2的实验方法是蒸馏.
(4)装置E中倒扣漏斗的作用是防止倒吸.
(5)S2Cl2易与水反应,有淡黄色沉淀生成,产生的无色气体能使品红溶液褪色,写出该反应的化学方程式2S2Cl2+2H2O=3S↓+SO2↑+4HCl.
8.分子式为C5H12O的醇有多种结构,其中能发生催化氧化生成醛的结构有(不考虑立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |

 某化学兴趣小组用FeCl2(用铁粉与盐酸反应制得)和NH4HCO3制备FeCO3的装置示意图如图所示.回答下列问题:
某化学兴趣小组用FeCl2(用铁粉与盐酸反应制得)和NH4HCO3制备FeCO3的装置示意图如图所示.回答下列问题: