题目内容
下列各项中的两种物质无论以何种比例混合,只要混合物的总物质的量一定.则完全燃烧时生成水的质量和消耗O2的质量均不变的是( )
| A、C3H6、C3H8O |
| B、C3H6、C2H6O |
| C、C2H2、C6H6 |
| D、CH4、C2H4O2 |
考点:有关混合物反应的计算
专题:烃及其衍生物的燃烧规律
分析:只要混合物的总物质的量一定,完全燃烧消耗O2的质量保持不变,则1mol各组分消耗氧气的量相等;总物质的量一定生成水的质量不变,则有机物分子中含有的H原子数目一定相等,据此进行解答.
解答:
解:混合物的总物质的量一定,完全燃烧生成水的质量和消耗O2的质量均不变,则1mol各组分消耗氧气的量相等,分子中含有的氢原子数目相等,
A.C3H6、C3H8O分子中含有的氢原子分别为6、8,二者含有的氢原子数不同,则不同比例混合后生成水的量不同,故A错误;
B.1molC3H6完全反应消耗4.5mol氧气,而1molC2H6O完全反应消耗3mol氧气,所以1molC3H6与1molC2H6O耗氧量不相同,不符合题意,故B错误;
C.C2H2、C6H6最简式相同,1molC6H6的耗氧量为1molC2H2耗氧量的3倍,且分子中含有的H数目不同,物质的量一定时二者比例不同,生成水的量不同,故C错误;
D.C2H4O2改写为CH4.CO2,CH4、C2H4O2分子中含有H原子数相等,且1mol时消耗的氧气都是2mol,所以只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变,故D正确;
故选D.
A.C3H6、C3H8O分子中含有的氢原子分别为6、8,二者含有的氢原子数不同,则不同比例混合后生成水的量不同,故A错误;
B.1molC3H6完全反应消耗4.5mol氧气,而1molC2H6O完全反应消耗3mol氧气,所以1molC3H6与1molC2H6O耗氧量不相同,不符合题意,故B错误;
C.C2H2、C6H6最简式相同,1molC6H6的耗氧量为1molC2H2耗氧量的3倍,且分子中含有的H数目不同,物质的量一定时二者比例不同,生成水的量不同,故C错误;
D.C2H4O2改写为CH4.CO2,CH4、C2H4O2分子中含有H原子数相等,且1mol时消耗的氧气都是2mol,所以只要混合物的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变,故D正确;
故选D.
点评:本题考查混合物计算、有机物分子式确定,难度不大,注意根据燃烧通式理解烃及其含氧衍生物耗氧量问题,注意利用改写法进行比较,避免计算的繁琐.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将两支惰性电极插入CuSO4溶液中,通电电解,当有1×10-3mol的OH-放电时,溶液显浅蓝色,则下列叙述正确的是( )
| A、阳极上析出5.6mL O2(标准状况) |
| B、阴极上析出64mg Cu |
| C、阴极上析出11.2mL H2(标准状况) |
| D、阳极和阴极质量都无变化 |
在水中加入等物质的量的Ag+、Ba2+、SO42-、NO3-、Cl-、Na+,用惰性材料作电极进行电解,通电片刻后停止,下列说法不正确的是( )
| A、电解的实质是:阳极:2Cl--2e-=Cl2↑;阴极:Ag+e-=Ag |
| B、电解的实质是:阳极:4OH--4e-=2H2O+O2↑;阴极:2H++2e-=H2↑ |
| C、要恢复成电解前的溶液可以加水 |
| D、电解产物中氧化产物和还原产物的物质的量之比为1:2 |
有Na2CO3、NaHCO3、CaO和NaOH组成的混合物27.2g,把它们溶于足量的水中,充分反应后,溶液中Ca2+、CO
、HCO
均转化为沉淀,将反应容器内水分蒸干,最后得白色固体物质共30.8g,则原混合物中含Na2CO3的质量是( )
2- 3 |
- 3 |
| A、10.6g | B、5.3g |
| C、21.6g | D、无法确定 |
当燃烧镁和某金属组成的合金时,所形成的氧化物的质量为反应前合金质量的2倍,则另一种金属可能是( )
| A、铜 | B、钠 | C、铍 | D、铝 |
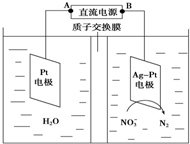 目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )
目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )| A、Pt电极为阴极 |
| B、电解过程中H+向正极移动 |
| C、理论上电解过程中阴、阳两极产生的气体在相同条件下体积比为2:5 |
| D、电解过程中Pt电极附近溶液的pH增大 |
下列检验某未知溶液中是否含有SO42-的操作中,最合理的是( )
| A、先加HCl酸化,再加BaCl2溶液 |
| B、加入HCl酸化了的BaCl2溶液 |
| C、先加HNO3酸化,再加Ba(NO3)2溶液 |
| D、加入HNO3酸化了的Ba(NO3)2溶液 |