题目内容
20.以下为中学化学中常见的物质:①Cu; ②1mol•L-1的FeCl3溶液; ③CuCl2溶液;④CO2;⑤H2SO4;⑥酒精;⑦CaCO3;⑧FeSO4(1)以上物质中属于电解质的是⑤⑦⑧;属于混合物的是②③.
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入②的溶液,至液体呈透明的红褐色氢氧化铁胶体.则反应的化学方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;氢氧化铁胶体中分散质微粒的直径范围为1~100nm;判断该胶体制备是否成功的方法是用一束光线照射,能产生一条光亮的通路.
(3)将②③⑧混合配制成浓度均为1mol•L-1的混合溶液100mL,加入一定量的铁粉,充分反应后,若铁粉无剩余,且有铜生成.则反应后的溶液中一定含有Fe2+阳离子,可能含有Cu2+阳离子,该阳离子在溶液中物质的量可能的存在范围是0.25mol<n(Fe2+)≤0.35mol.
分析 (1)在水溶液中或熔融状态下能导电的化合物为电解质;由两种或以上物质构成的为混合物;
(2)本题要根据氢氧化铁胶体胶体的制备、性质(丁达尔效应、聚沉)和胶体微粒直径的大小解答;
(3)FeCl3、CuCl2和FeSO4的混合溶液中加入铁粉,铁粉先和Fe3+反应,然后再和Cu2+反应,当铁粉无剩余、且有铜生成时,说明Fe3+反应完全,Cu2+已经开始反应,而铁粉无剩余,故Cu2+不一定完全反应,据此分析.
解答 解:(1)①Cu是单质,是纯净物,既不是电解质也不是非电解质; ②1mol•L-1的FeCl3溶液是混合物,既不是电解质也不是非电解质; ③CuCl2溶液是混合物,既不是电解质也不是非电解质;④CO2是纯净物,是非电解质;⑤H2SO4是纯净物,是电解质;⑥酒精是纯净物,是非电解质;⑦CaCO3是纯净物,是电解质;⑧FeSO4
是纯净物,是电解质,故是电解质的是⑤⑦⑧;是混合物的是②③,
故答案为:⑤⑦⑧;②③;
(2))制备氢氧化铁胶体用的水眼泪水解的知识,加热条件下FeCl3的水解生成胶体,因此方程式中要写明条件(加热),特别注意的是:生成的是胶体而不是沉淀,化学方程式为FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;氢氧化铁胶体是胶体分散系中的一种,胶体粒子直径大小在1nm~100nm;胶体区别于溶液的关键在于:溶液粒子直径小于1nm,胶体粒子直径大小在1nm~100nm,即溶液不产生丁达尔效应,而氢氧化铁胶体能产生丁达尔效应,
故答案为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;1~100;用一束光线照射,能产生一条光亮的通路;
(3)当有铜生成,铁粉无剩余,溶液中一定没有Fe3+,Cu2+恰好全部参加反应或部分反应生成Fe2+和Cu,所以溶液中一定没有Fe3+,可能含有Cu2+,一定含有Fe2+;
如果只有Fe2+,则其物质的量为:0.35mol,如果还有Cu2+,且最多为0.1mol时,只发生2FeCl3+Fe=3FeCl2,则Fe2+物质的量为0.25mol,由于两个反应都发生,所以Cu2+小于0.1mol,因此Fe2+物质的量大于0.25mol,故Fe2+物质的量为:0.25mol<n(Fe2+)≤0.35mol,
故答案为:Fe2+;Cu2+;0.25mol<n(Fe2+)≤0.35mol.
点评 本题考查了电解质非电解质的判断、混合物和纯净物的判断以及Fe与Fe3+、Cu2+的反应,熟悉三价铁离子、铜离子氧化性强弱是解题关键,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | 氢氧化铜与盐酸的反应 Cu(OH)2+2H+=Cu2++2 H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag | |
| D. | 碳酸钙溶于盐酸中 CaCO3+H+=Ca2++H2O+CO2↑ |
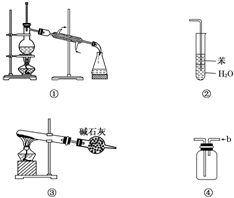
| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收氨气,能够防止倒吸 | |
| C. | 以NH4HCO3为原料,装置③可用于制备少量CO2 | |
| D. | 装置④a口进气可收集Cl2、NO2等气体 |
| A. | Na+、Mg2+、Cl-、SO42- | B. | Cu2+、Cl-、NO3-、OH- | ||
| C. | Ca2+、Na+、CO32-、NO3- | D. | K+、Fe3+、NO3-、SCN- |
| A. | ②④⑥ | B. | ①③④ | C. | ①③⑤⑥ | D. | ②⑤ |
(1)写出F原子的外围电子排布式3d64s2.
| 元 素 | M | F | |
| 电离能 (kJ•mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(3)F和M(质子数为25)两元素的部分电离能数据列于右表:比较两元素的I2、I3可知,气态M2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是:Mn2+的3d轨道电子排布为半满状态较稳定.
(4)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
(5)如图a、b分别为M、F晶体的堆积模型,假设M的原子半径分别为Ranm,它的空间利用率:(不用化简)M$\frac{π}{3\sqrt{2}}$.

| A. | 铜是负极,铜片上有气泡产生 | B. | 电流从锌片经导线流向铜片 | ||
| C. | H+在铜片表面被还原 | D. | 铜片质量逐渐减小 |