题目内容
一定能在下列溶液中大量共存的离子组是( )
| A、含有大量Fe3+的溶液:Na+、SCN-、OH-、NO3- |
| B、碱性溶液:K+、Ca2+、Cl-、CO32- |
| C、酸性溶液:Na+、NH4+、SO42-、Cl- |
| D、含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
考点:离子共存问题
专题:
分析:A.与Fe3+反应的离子不能大量共存;
B.生成沉淀的离子不能大量共存;
C.如离子之间不发生任何反应,可大量共存;
D.酸性条件下,NO3-具有强氧化性,可与还原性物质发生氧化还原反应.
B.生成沉淀的离子不能大量共存;
C.如离子之间不发生任何反应,可大量共存;
D.酸性条件下,NO3-具有强氧化性,可与还原性物质发生氧化还原反应.
解答:
解:A.SCN-、OH-与Fe3+反应而不能大量共存,故A错误;
B.Ca2+、CO32-生成沉淀,不能大量共存,故B错误;
C.酸性条件下,离子之间不发生任何反应,可大量共存,故C正确;
D.酸性条件下,NO3-具有强氧化性,可与Fe2+发生氧化还原反应,故D错误.
故选C.
B.Ca2+、CO32-生成沉淀,不能大量共存,故B错误;
C.酸性条件下,离子之间不发生任何反应,可大量共存,故C正确;
D.酸性条件下,NO3-具有强氧化性,可与Fe2+发生氧化还原反应,故D错误.
故选C.
点评:本题考查离子共存问题,为高频考点,题目难度中等,本题注意把握相关题给信息,为解答该类题目的关键,学习中注重相关基础知识的积累.

练习册系列答案
相关题目
下列说法正确的是( )
| A、向蒸馏水中滴加浓H2SO4时,KW不变 |
| B、常温下,0.005mol?L-1Ba(OH)2溶液pH为12 |
| C、NaHCO3水解的离子方程式为:HCO3-+H2O?CO32-+H3O+ |
| D、NaHSO3属于强碱弱酸盐,其水溶液一定显碱性 |
下列说法中正确的是( )
| A、石油分馏、煤的干馏均是物理变化 |
| B、PM2.5是指氮、硫的氧化物溶于水形成的酸性液体造成的空气污染 |
| C、资源的“3R”即减少消耗(Reduce)、增加重复使用(Reuse)、重复再生(Recycle)有利于实现“低碳生活” |
| D、铅蓄电池、锂电池、碱性锌锰干电池都属于二次电池 |
物质间常常相互联系、互相影响着,微粒也不例外.下列各组离子可能大量共存的是( )
| A、不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、C1O-、I- |
| B、能与金属铝反应放出氢气的溶液中:K+、NO3-、C1-、NH4+ |
| C、常温下水电离出的c(H+)?c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- |
| D、无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+ |
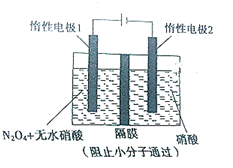 用如图装置电解制备N2O5 ,下列有关说法正确的是( )
用如图装置电解制备N2O5 ,下列有关说法正确的是( )| A、N2O5在惰性电极2处产生 |
| B、在惰性电极2处有氢气产生 |
| C、在惰性电极1处发生还原反应 |
| D、在惰性电极2处有NO产生 |
下列各组离子,能在溶液中大量共存的是( )
| A、Na+、Cu2+、Cl-、SO42- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、K+、H+、SO42-、OH- |
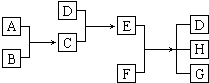 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示: