题目内容
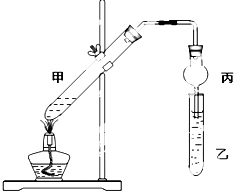 如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓慢加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸.将试管甲固定在铁架台上,在试管乙中加入5mL饱和碳酸钠溶液,按如图连接好装置进行实验,当试管乙中有明显现象时停止实验.
如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓慢加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸.将试管甲固定在铁架台上,在试管乙中加入5mL饱和碳酸钠溶液,按如图连接好装置进行实验,当试管乙中有明显现象时停止实验.试回答:
(1)实验时,应对试管甲缓慢加热,其目的是
(2)写出试管甲中发生反应的化学方程式
(3)加入浓硫酸的作用是
(4)该实验中球形管丙的作用是
(5)饱和碳酸钠作用
(6)某同学做此实验时,观察到反应混合液变黑,并闻到刺激性气味,试分析其原因
考点:乙酸乙酯的制取
专题:实验题
分析:(1)乙醇和乙酸都具有挥发性,温度高,挥发快且有副反应发生;
(2)装置中发生的反应是醋酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水;
(3)浓硫酸做酯化反应的催化剂和吸水剂;
(4)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用;
(5)实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:一是利用碳酸钠溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,这样就可以获得较为纯净的乙酸乙酯液体;
(6)浓硫酸具有脱水性,能把乙醇脱水生成碳,本身被还原为二氧化硫.
(2)装置中发生的反应是醋酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水;
(3)浓硫酸做酯化反应的催化剂和吸水剂;
(4)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用;
(5)实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:一是利用碳酸钠溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,这样就可以获得较为纯净的乙酸乙酯液体;
(6)浓硫酸具有脱水性,能把乙醇脱水生成碳,本身被还原为二氧化硫.
解答:
解:(1)乙醇和乙酸都具有挥发性,为了减少挥发,要缓慢加热,温度高时,浓硫酸可把乙醇氧化;
故答案为:减少乙醇乙酸的挥发,减少副反应发生;
(2)装置中发生的反应是醋酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;
故答案为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;
(3)浓硫酸有吸水性,促进该反应向正反应方向移动,浓硫酸能加快反应速率,所以浓硫酸作催化剂和吸水剂;故答案为:催化剂 吸水剂;
(4)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用;
故答案为:防倒吸;
(5)碳酸钠溶液中的水溶解乙醇,能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,降低乙酸乙酯的溶解度,使乙酸乙酯难溶于饱和碳酸钠溶液,便于分层;
故答案为:吸收乙醇,中和乙酸,降低乙酸乙酯的溶解度;
(6)温度高时,浓硫酸使乙醇脱水有碳生成,浓硫酸被还原为二氧化硫,故看到混合液变黑,并闻到刺激性气味;
故答案为:温度高时,浓硫酸使乙醇脱水有碳生成,浓硫酸被还原为二氧化硫.
故答案为:减少乙醇乙酸的挥发,减少副反应发生;
(2)装置中发生的反应是醋酸和乙醇在浓硫酸催化作用下发生酯化反应,生成乙酸乙酯和水,反应的化学方程式为:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
(3)浓硫酸有吸水性,促进该反应向正反应方向移动,浓硫酸能加快反应速率,所以浓硫酸作催化剂和吸水剂;故答案为:催化剂 吸水剂;
(4)乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用;
故答案为:防倒吸;
(5)碳酸钠溶液中的水溶解乙醇,能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,降低乙酸乙酯的溶解度,使乙酸乙酯难溶于饱和碳酸钠溶液,便于分层;
故答案为:吸收乙醇,中和乙酸,降低乙酸乙酯的溶解度;
(6)温度高时,浓硫酸使乙醇脱水有碳生成,浓硫酸被还原为二氧化硫,故看到混合液变黑,并闻到刺激性气味;
故答案为:温度高时,浓硫酸使乙醇脱水有碳生成,浓硫酸被还原为二氧化硫.
点评:本题考查乙酸乙酯的制备,题目难度不大,本题注意把握乙酸乙酯的制备原理和实验方法,学习中注重实验评价能力的培养.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
若将7N原子的电子排布图画成 ,它违背了( )
,它违背了( )
 ,它违背了( )
,它违背了( )| A、能量守恒原理 |
| B、泡利不相容原理 |
| C、洪特规则 |
| D、能量最低原理 |
某学生在实验室制取乙酸乙酯(反应温度80℃左右)和乙酸丁酯(反应温度115~125℃),现有两套实验装置图Ⅰ和图Ⅱ.下列说法错误的是( )
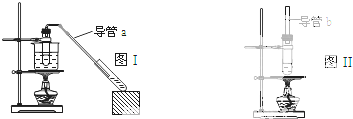

| A、制乙酸乙酯用图I装置,制乙酸丁酯用图II 装置 |
| B、导管a和导管b的作用都是冷凝回流 |
| C、都可用Na2CO3 溶液来洗去酯中的酸和醇 |
| D、加入过量的乙酸可以提高醇的转化率 |
已知某元素原子的各级电离能( kJ?mol-1)数值如下表,则该原子最外层的电子数为( )
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 577 | 1820 | 2740 | 11600 | 14800 | 18400 | 23400 |
| A、1 | B、3 | C、5 | D、7 |
下列说法正确的是( )
| A、BeCl2分子中各原子最外层均已满足8电子稳定结构 |
| B、第ⅡA族的某元素原子序数为x,则原子序数为x+1的元素不一定在第ⅢA族 |
| C、构成单质分子的粒子间一定存在化学键 |
| D、含有离子键的化合物不一定是离子化合物 |
已知某元素+3价离子的电子排布为:1s22s22p63s23p63d5,该元素在周期表中的位置正确的是( )
| A、第三周期Ⅷ族,p区 |
| B、第三周期ⅤB族,ds区 |
| C、第四周期Ⅷ族,d区 |
| D、第四周期ⅤB族,f区 |
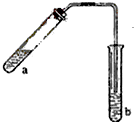 哈三中某化学课外学习小组利用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空:
哈三中某化学课外学习小组利用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空: