题目内容
下列有关热化学方程式正确的是(在25℃、101KPa下)( )
| A、S(s)+O2(g)=SO2(g);△H=-297.23kJ?mol-1 |
| B、2H2(g)+O2(g)=2H2O(1);△H=-571.6 kJ |
| C、CaCO3(s)=CaO(s)+CO2(g);△H=178.5 kJ?mol |
| D、Zn+CuSO4(aq)=ZnSO4(aq)+Cu;△H=-216kJ?mol-1 |
考点:热化学方程式
专题:
分析:A、S(s)+O2(g)=SO2(g);△H=-297.23kJ?mol-1;
B、反应热的单位kJ?mol-1;
C、反应热的单位kJ?mol-1;
D、物质聚集状态未标注.
B、反应热的单位kJ?mol-1;
C、反应热的单位kJ?mol-1;
D、物质聚集状态未标注.
解答:
解:A、S(s)+O2(g)=SO2(g);△H=-297.23kJ?mol-1,故A正确;
B、反应热的单位kJ?mol-1,故B错误;
C、吸热反应符号为“+”,反应热的单位kJ?mol-1,故C错误;
D、物质聚集状态未标注,故D错误;
故选A.
B、反应热的单位kJ?mol-1,故B错误;
C、吸热反应符号为“+”,反应热的单位kJ?mol-1,故C错误;
D、物质聚集状态未标注,故D错误;
故选A.
点评:本题主要考查热化学方程式的书写方法及系数的含义,注意焓变的正负和物质的状态.

练习册系列答案
相关题目
下列实验操作与安全事故处理正确的是( )
| A、金属钠着火时可用干粉灭火器扑灭 |
| B、在硫酸铜晶体结晶水含量测定的实验中,称量操作至少需要四次 |
| C、铜与浓硫酸反应时,用蘸有浓溴水的棉花放在导管口吸收多余的气体 |
| D、在250 mL烧杯中加入216 mL水和24 g NaOH固体,配制10%NaOH溶液 |
下列各种情况下,溶液中可能大量存在的离子组是( )
| A、由水电离出的c(H+)=l×10-12mol/L、的溶液中:K+、Ba2+、OH-、NO3- |
| B、澄清透明的溶液中:I-、Cl-、ClO-、Na+ |
| C、使pH试纸呈红色的溶液中:K+、Fe2+、NO3-、MnO4- |
| D、含有S2O32-的溶液中:K+、Na+、H+、SO42- |
下列各组物质中,不能满足“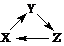 ”转化关系的一组是
”转化关系的一组是
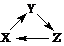 ”转化关系的一组是
”转化关系的一组是| X | Y | Z | |
| A | CH2=CH2 | CH3CH2OH | CH3CH2Br |
| B | CH3CH2OH | CH3CHO | CH3COOH |
| C | C | CO | CO2 |
| D | HNO3 | NO | NO2 |
| A、A | B、B | C、C | D、D |
尼泊金酯是对羟基苯甲酸  与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
 与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )| A、尼泊金乙酯与NaOH溶液反应时,可消耗1mol NaOH |
| B、尼泊金乙酯分子结构中,至少有6个碳原子在一个平面内 |
| C、尼泊金丁酯最多可与4mol H2发生加成反应 |
D、尼泊金丁酯是由对羟基苯甲酸与1-丁醇形成的酯,结构简式如图: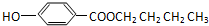 |