题目内容
下列叙述正确的是( )
| A、1mol H2O的质量为18g?mol-1 |
| B、CO2的摩尔质量为44g |
| C、3.01×1023个SO2分子的质量为32g |
| D、64g氧气中含有2mol氧 |
考点:物质的量的相关计算
专题:计算题
分析:A.质量的常用单位为克,g?mol-1为摩尔质量的单位;
B.摩尔质量的单位为g?mol-1;
C.根据n=
和m=nM计算;
D.2mol氧表述不清;
B.摩尔质量的单位为g?mol-1;
C.根据n=
| N |
| NA |
D.2mol氧表述不清;
解答:
解:A.根据m=nM=1mol×18g/mol=18g,故A错误;
B.摩尔质量的单位为g/mol,在数值上等于该物质的相对分子质量,因此CO2的摩尔质量是44g/mol,故B错误;
C.3.01×1023个SO2分子n=
=
=0.5mol,m=nM=0.5mol×64g/mol=32g,故C正确;
D.64g氧气的物质的量是
=2mol,氧气为双原子分子,故含氧原子为4mol,2mol氧表述不清,是指氧原子还是氧分子,不明确,故D错误;
故选C.
B.摩尔质量的单位为g/mol,在数值上等于该物质的相对分子质量,因此CO2的摩尔质量是44g/mol,故B错误;
C.3.01×1023个SO2分子n=
| N |
| NA |
| 3.01×1023 |
| 6.02×1023 |
D.64g氧气的物质的量是
| 64g |
| 32g/mol |
故选C.
点评:本题考查了以物质的量为中心的计算,较基础,注意物质的量单位摩尔后要带具体的化学式,掌握摩尔质量的含义是解答本题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将质量分数为a%,物质的量浓度为c1 mol?L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol?L-1,则c1和c2的数值关系是( )
| A、c2=c1 |
| B、c2<2c1 |
| C、c2>2c1 |
| D、c2=2c1 |
下列关于氯水的叙述,不正确的是( )
| A、新制氯水中只含有Cl2和H2O分子 |
| B、加入AgNO3溶液有白色沉淀产生 |
| C、光照氯水有气泡逸出,久置的氯水,酸性增强 |
| D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |
下列反应不属于可逆反应的是( )
| A、氯气溶于水 | |||
| B、氨气溶于水 | |||
C、可充电电池的反应如2Ag+Zn(OH)2
| |||
| D、工业合成氨 |
下列物质中,属于含有极性共价键的离子化合物的是( )
| A、HCl |
| B、NaCl |
| C、NaOH |
| D、CO2 |
下列物质属于纯净物的是( )
| A、生铁 | B、钢 |
| C、赤铁矿 | D、磁性氧化铁 |
环境、能源和资源是人类面临的三大问题.下列关于能源和环境的说法中,不正确的是( )
| A、凡是能提供能量的资源都是能源 |
| B、解决能源危机的有效办法包括提高能源利用率、寻找新能源等 |
| C、化石燃料不可再生、易产生污染,且储量有限,是一种有局限性的能源 |
| D、雾霾中含有大量的PM2.5可吸入颗粒,汽车尾气与雾霾的形成无关 |
在容积不变的密闭容器中存在如下反应2SO2(g)+O2(g)?2SO3(g)△H<0,某研究小组探究其他条件下不变时,改变某一条件对上述反应的影响,下列分析正确的是( )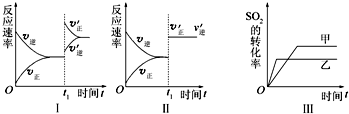

| A、图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B、图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响 |
| C、图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙的高 |
| D、图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |