题目内容
19.W、X、Y、Z为原子序数依次增加的短周期主族元素,它们的电子层数之和为9,它们的族序数之和为19,其中X的最高价氧化物对应的水化物能与W、X形成的简单化合物化合生成盐M.下列说法正确的是( )| A. | 单质的沸点:Y<X | B. | 简单离子半径:Y<Z | ||
| C. | 盐M的水溶液显酸性 | D. | 最高化合价:X>Y>Z |
分析 X的最高价氧化物对应的水化物能与W、X形成的简单化合物化合生成盐M,则X只能为N元素,M为硝酸铵,所以W为H;再根据W、X、Y、Z的电子层数之和为9,它们的族序数之和为19,则Y、Z的电子层数之和为:9-1-2=6,二者为短周期元素,则Y、Z都处于第三周期;Y、Z的族序数为:19-1-5=13,由于都是主族元素,则Y为S、Z为Cl元素,据此进行解答.
解答 解:X的最高价氧化物对应的水化物能与W、X形成的简单化合物化合生成盐M,则X只能为N元素,M为硝酸铵,所以W为H;再根据W、X、Y、Z的电子层数之和为9,它们的族序数之和为19,则Y、Z的电子层数之和为:9-1-2=6,二者为短周期元素,则Y、Z都处于第三周期;Y、Z的族序数为:19-1-5=13,由于都是主族元素,则Y为S、Z为Cl元素,
A.X为N、Y为S,对应单质为S和氮气,氮气的沸点小于S,即:Y>X,故A错误;
B.Y为S、Z为Cl元素,对应离子为硫离子、氯离子,二者电子层数相同,核电荷数越大,离子半径越小,则硫离子的离子半径大于氯离子,即:Y>Z,故B错误;
C.M为硝酸铵,铵根离子部分水解,溶液呈酸性,故C正确;
D.X为H、Y为N、Z为Cl,其最高化合价分别为+1、+5、+7,则最高化合价大小为:X<Y<Z,故D错误;
故选C.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,根据“X的最高价氧化物对应的水化物能与W、X形成的简单化合物化合生成盐M”推断X为N元素为突破口,注意掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
相关题目
9.下列数值都是烃的相对分子质量,其对应的烃一定是烷烃的是( )
| A. | 44 | B. | 42 | C. | 54 | D. | 128 |
10.下列反应过程能量变化如下所示:
H2(g)+Cl2(g)═2HCl(g)△H
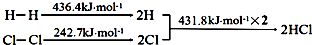
下列说法错误的是( )
H2(g)+Cl2(g)═2HCl(g)△H
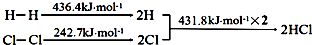
下列说法错误的是( )
| A. | H-H键比Cl-Cl键稳定 | |
| B. | △H=-184.5 kJ•mol-1 | |
| C. | 正反应活化能比逆反应活化能高 | |
| D. | 在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时△H相同 |
14.设NA表示阿伏伽德罗常数的值,下列叙述中不正确的是( )
| A. | 室温下,46gNO2和N2O4的混合气体中含有NA个氮原子 | |
| B. | 1mol12C18O2中所含的中子数为26NA | |
| C. | 常温下,1L0.1mol/LCH3COONa溶液中含有CH3COO-和Na+总数为0.2NA | |
| D. | 常温下,1LpH=12的氨水中含有OH-的数目为0.01NA |
4.将20mL0.8mol•L-1H2SO4溶液加水稀释到100mL,稀释后H2SO4溶液中的物质的量浓度为( )
| A. | 0.2mol•L-1 | B. | 0.16mol•L-1 | C. | 0.32mol•L-1 | D. | 0.08mol•L-1 |
8.莫尔盐[(NH4)2Fe(SO4)2•6H2O]常作氧化还原滴定法的基准物质,在0.1mol/L 的该盐的溶液中,下列有关比较正确的是( )
| A. | c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | B. | c(H+)=c(OH-)+c(NH3•H2O) | ||
| C. | c(SO42-)+c(OH-)=c(NH4+)+c(Fe2+)+c(H+) | D. | c(NH3•H2O)+c(NH4+)=0.1 mol/L |
 取6根铁钉,6支干净的试管及其他材料,如图所示.
取6根铁钉,6支干净的试管及其他材料,如图所示. ;SO3的沸点为44.8℃,其汽化时需克服的作用力是分子间作用力.
;SO3的沸点为44.8℃,其汽化时需克服的作用力是分子间作用力.