题目内容
6. 将铁片和碳棒按图示方式插入硫酸铜溶液中,电流计指针发生偏转.下列针对该装置的说法,正确的是( )
将铁片和碳棒按图示方式插入硫酸铜溶液中,电流计指针发生偏转.下列针对该装置的说法,正确的是( )| A. | 碳棒是负极 | |
| B. | 该装置能将电能转化为化学能 | |
| C. | 外电路中电流由铁片流出经过电流计流向碳棒 | |
| D. | 该装置的总反应为:Fe+Cu2+=Fe2++Cu |
分析 该装置能自发的进行氧化还原反应,能将化学能转化为电能,属于原电池,Fe易失电子作负极、C作正极,负极反应式为Fe-2e-=Fe2+、正极反应式为Cu2++2e-=Cu,电子从负极沿导线流向正极,据此分析解答.
解答 解:A.Fe易失电子作负极、C作正极,故A错误;
B.该装置是将化学能转化为电能的装置,属于原电池,故B错误;
C.该装置中Fe易失电子作负极、C作正极,电流由碳棒流出经过电流计流向铁片,故C错误;
D.该装置电池反应式与Fe和硫酸铜发生置换反应方程式相同为Fe+Cu2+=Fe2++Cu,故D正确;
故选D.
点评 本题考查了原电池原理,根据能量转化方式确定装置类型,再结合正负极上发生的反应及电子流向分析解答,知道原电池正负极的判断方法,题目难度不大.

练习册系列答案
相关题目
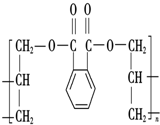
4.对于反应: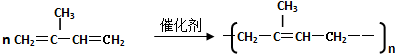 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该反应的类型是缩聚反应 | |
| B. | 产物中链节的式量比反应物单体的分子量大 | |
| C. | 工业上用该反应生产顺丁橡胶 | |
| D. | 不同产物分子的聚合度可能不同 |
14.一定条件下,某反应达到平衡,其平衡常数为 K=$\frac{c(C{O}_{2})•c(NO)}{c(N{O}_{2})•c(CO)}$恒容时升高温度,混合气体的颜色加深,下列说法不正确的是( )
| A. | 该反应的焓变为负值 | |
| B. | 化学方程式为 NO2(g)+CO(g)?CO2(g)+NO(g) | |
| C. | 降温,正反应速率减小 | |
| D. | 恒温时,增大压强颜色加深,平衡逆向移动 |
1.实现下列变化时,需克服相同类型作用力的是( )
| A. | 金刚石和干冰的熔化 | B. | 纯碱和烧碱的熔化 | ||
| C. | 氯化铵和水的分解 | D. | 食盐和冰醋酸熔化 |
11.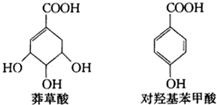 以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )
以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )
 以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )
以莽草酸为原料,经多步反应可制取对羟基苯甲酸.莽草酸、对羟基苯甲酸的结构简式如图.下列说法正确的是( )| A. | 莽草酸、对羟基苯甲酸都属于芳香族化合物 | |
| B. | 1mol莽草酸与NaOH溶液反应,最多消耗4 mol NaOH | |
| C. | 利用FeCl3溶液可鉴别莽草酸和对羟基苯甲酸 | |
| D. | 对羟基苯甲酸较稳定,在空气中不易被氧化 |
18.下列说法正确的是( )
| A. | C与Si位于同一主族,且干冰与SiO2都是酸性氧化物,所以二者晶体类型相同 | |
| B. | NaCl和AlCl3均为强电解质,二者在熔融状态下都能导电 | |
| C. | 从晶体类型上来看物质的熔沸点,其规律是:原子晶体>离子晶体>分子晶体 | |
| D. | 第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 |
15.下列有关甲烷的叙述正确的是( )
| A. | 天然气的主要成分甲烷燃烧时放出大量热量,属于重要的二次能源 | |
| B. | 甲烷分子中四个碳氢单键的性质完全相同,分子结构为平面正方形 | |
| C. | 甲烷和氯气反应生成的二氯甲烷没有同分异构现象 | |
| D. | 甲烷的化学性质比较稳定,不被任何氧化剂氧化 |
16.下列反应过程中,先有沉淀生成,后沉淀又会消失的是( )
| A. | 将氨水逐滴滴入Al2(SO4)3溶液中,直至过量 | |
| B. | 在AlCl3溶液中逐滴滴入NaOH溶液,直至过量 | |
| C. | 在NaOH 溶液中逐滴滴入 MgSO4 溶液,直至过量 | |
| D. | 在 Na2SiO3溶液中逐滴滴入盐酸,直至过量 |