题目内容
某原子的摩尔质量是Mg?mol-1,则一个该原子的真实质量是( )
| A、Mg | ||
B、
| ||
C、
| ||
| D、6.02×1023 Mg |
考点:物质的量的相关计算
专题:计算题
分析:由摩尔质量可知1mol原子质量为M g,1mol原子的数目为 6.02×10-23个,据此计算一个原子的质量.
解答:
解:原子的摩尔质量是Mg?mol-1,1mol原子质量为M g,1mol原子的数目为 6.02×10-23个,故一个原子的质量为:
g,故选C.
| M |
| 6.02×1023 |
点评:本题考查摩尔质量、阿伏伽德罗常数等,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
 右图是元素周期表中的某一种元素的信息,下列有关该元素的信息不正确的是( )
右图是元素周期表中的某一种元素的信息,下列有关该元素的信息不正确的是( )| A、原子序数是 13 |
| B、它是非金属元素 |
C、离子结构示意图为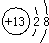 |
| D、相对原子质量是26.98 |
对比甲烷和乙烯的燃烧反应,下列叙述中正确的是( )
| A、二者燃烧时现象完全相同 |
| B、点燃前都应验纯 |
| C、甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮 |
| D、二者燃烧时都有黑烟生成 |
下列关于胶体的叙述,正确的是( )
| A、胶体区别于其他分散系的本质特征是分散质的微粒直径大于10-7m |
| B、制备氢氧化铁胶体的化学方程式是:FeCl3+3H2O═Fe(OH)3↓+3HCl |
| C、用平行光照射NaCl溶液和氢氧化铁胶体时,产生的现象相同 |
| D、氢氧化铁胶体能够使水中悬浮的固体颗粒沉降,达到净水的目的 |
下列说法中正确的是( )
| A、在20℃,1.01×105Pa时,11.2L氧气所含的原子数为NA |
| B、0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA |
| C、在标准状况下,2mol酒精的体积约为44.8L |
| D、常温常压下,质量为32g的O2含有的分子数为NA |
设NA 为阿伏伽德罗常数的数值,下列说法不正确的是( )
| A、39gC2H2和C6H6混合物中含有的原子数为6NA |
| B、标准状况下,以任意比例混和的CO和C2H4混和物22.4L,所含有的原子数为2NA |
| C、23g甲酸中所含的共用电子对数为2.5NA |
| D、7.1gCl2与足量的NaOH溶液发生反应,电子转移数为0.1 NA |
下列物质在空气中,久置若变质,在变质过程中,既有氧化还原反应,又有非氧化还原反应发生的是( )
| A、食盐 | B、漂白粉 | C、氯水 | D、胆矾 |
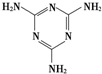 (双项)三聚氰胺(结构式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )
(双项)三聚氰胺(结构式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )| A、三聚氰胺不属于蛋白质 |
| B、三聚氰胺是高分子化合物 |
| C、三聚氰胺分子中含有碳碳双键 |
| D、三聚氰胺的分子式为C3H6N6 |