题目内容
20.CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g)△H1=+218.4kJ•mol-1(反应Ⅰ)CaSO4(s)+4CO(g)?CaS(s)+4CO2(g)△H2=-175.6kJ•mol-1(反应Ⅱ)
请回答下列问题:
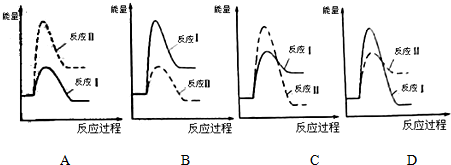
(1)假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则说明Ⅰ的活化能<Ⅱ的活化能(填><=)下列反应过程能量变化示意图正确的是C.
(2)已知25℃时中和热的△H=-57.3kJ/mol,反应Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l)
△H=-154.6kJ/mol,写出1mol BaSO4固体的溶解平衡的热化学方程式:Ba SO4 (s)
 Ba 2+(aq)+SO4 2-(aq)△H=+40KJ/mol.
Ba 2+(aq)+SO4 2-(aq)△H=+40KJ/mol.
分析 (1)反应速率越快,活化能越低;反应Ⅰ为吸热反应,反应物总能量小于生成物总能量,反应Ⅱ为放热反应,反应物总能量大于成物总能量;
(2)中和热的△H=-57.3kJ/mol,则①:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,
又知②:Ba 2+(aq)+2OH-(aq)+2H+(aq)+SO4 2-(aq)=BaSO4(s)+2H2O(l)△H=-154.6kJ/mol,
根据盖斯定律,①×2-②可得:Ba SO4 (s)  Ba 2+(aq)+SO4 2-(aq).
Ba 2+(aq)+SO4 2-(aq).
解答 解:(1)反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),反应速率越快,活化能越低,则说明Ⅰ的活化能<Ⅱ的活化能,
反应Ⅰ为吸热反应,反应物总能量小于生成物总能量,反应Ⅱ为放热反应,反应物总能量大于成物总能量,则A、D错误,Ⅰ的活化能<Ⅱ的活化能,则B错误、C正确,
故答案为:<;C;
(2)中和热的△H=-57.3kJ/mol,则①:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,
又知②:Ba 2+(aq)+2OH-(aq)+2H+(aq)+SO4 2-(aq)=BaSO4(s)+2H2O(l)△H=-154.6kJ/mol,
根据盖斯定律,①×2-②可得:Ba SO4 (s)  Ba 2+(aq)+SO4 2-(aq),△H=2×(-57.3kJ/mol)-(-154.6kJ/mol)=+40kJ/mol,
Ba 2+(aq)+SO4 2-(aq),△H=2×(-57.3kJ/mol)-(-154.6kJ/mol)=+40kJ/mol,
故答案为:Ba SO4 (s)  Ba 2+(aq)+SO4 2-(aq)△H=+40KJ/mol.
Ba 2+(aq)+SO4 2-(aq)△H=+40KJ/mol.
点评 本题考查化学反应能量变化图象、吸热反应与放热反应、热化学方程式书写,注意盖斯定律的理解与应用,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.相同物质的量浓度的下列物质的稀溶液中,pH最大的是( )
| A. | 乙醇 | B. | 乙酸钠 | C. | 苯酚钠 | D. | 碳酸钠 |
8.有机物 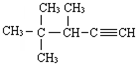 的系统名称为( )
的系统名称为( )
 的系统名称为( )
的系统名称为( )| A. | 2,2,3一三甲基一1-戊炔 | B. | 3,4,4一三甲基一l一戊炔 | ||
| C. | 3,4,4一三甲基-2一戊炔 | D. | 2,2,3一三甲基一4一戊炔 |
5.下列气体中,既能用浓硫酸也能用固体NaOH干燥的是( )
| A. | N2 | B. | SO2 | C. | NH3 | D. | Cl2 |
9.2011年11月,“神舟八号”在酒泉发射升空,并取得圆满成功.“神舟八号”的运载火箭所用燃料是偏二甲肼(C2H8N2)(其中N的化合价为-3)和四氧化二氮(N2O4).在火箭升空过程中,燃料发生反应:C2H8N2+2N2O4→2CO2+3N2+4H2O提供能量.下列有关叙述正确的是( )
| A. | 该燃料绿色环保,在燃烧过程中不会造成任何环境污染 | |
| B. | 该反应中N2O4是氧化剂,偏二甲肼是还原剂 | |
| C. | N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物 | |
| D. | 每有0.6 mol N2生成,转移电子数目为2.4NA |
10.下列各组中的离子,能在溶液中大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Ca2+、Na+、NO3-、CO32- | ||
| C. | Na+、H+、CO32-、Cl- | D. | Na+、Cl-、SO42-、Cl- |
 ;
;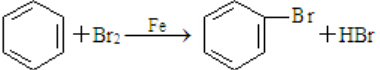 ;
;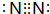 .
.