题目内容
20.电化学原理在化学工业中有广泛的应用.请根据如图回答问题:(1)装置Ⅰ中的X电极的名称是负极,Y电极的电极反应式为O2+2H2O+4e-=4OH-,工作一段时间后,电解液的PH将减小(填“增大”、“减小”、“不变”).
(2)若装置Ⅱ中a、b均为Pt电极,W为饱和食盐水(滴有几滴酚酞),实验开始后,观察到b电极周围溶液变红色,其原因是(用电极反应式表示)2H++2e-=H2↑,a电极上有气泡产生,该气体的电子式为
 .
.(3)若利用装置Ⅱ进行铜的精炼,则a电极的材料为粗铜,工作一段时间后装置Ⅱ电解液中c(Cu2+)将减小(填“增大”、“减小”、“不变”).
(4)若装置Ⅱ中a为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.16g,则流经电路的电子的物质的量为0.02mol.

分析 (1)装置Ⅰ为甲烷燃料电池,燃料在负极发生氧化反应,生成二氧化碳能够与KOH反应,导致溶液pH减小,氧气在正极发生还原反应,生成氢氧根离子;
(2)根据图知,Y是正极,b是阳极,用惰性电极电解饱和食盐水时,阴极上氢离子放电生成氢气,同时生成了氢氧根离子,溶液滴有酚酞的溶液显示红色;
(3)铜的电解精炼中,粗铜接阳极,因为阳极上有比铜活泼的金属放电,导致铜离子浓度减小;
(4)装置为电镀装置,铜棒增重2.16g,为Ag的质量,据此计算电子转移.
解答 解:(1)装置Ⅰ为甲烷燃料电池,燃料在负极发生氧化反应,生成二氧化碳能够与KOH反应,导致溶液pH减小,在碱性环境中,氧气在正极发生还原反应,生成氢氧根离子,电极反应式为:O2+2H2O+4e-=4OH-,故答案为:负极;O2+2H2O+4e-=4OH-;减小;
(2)电解饱和食盐水得到氢气、氯气和氢氧化钠,阴极上氢离子放电生成氢气,同时电极附近生成氢氧化钠,所以溶液碱性增强,酚酞试液遇碱变红色,电极反应式为:2H++2e-=H2↑,氯气的电子式为 ,故答案为:2H++2e-=H2↑;
,故答案为:2H++2e-=H2↑; ;
;
(3)电镀法精炼铜时,粗铜为阳极,精铜为阴极,所以阳极材料是粗铜;阳极上失电子变成离子进入溶液,因作阳极的粗铜中的铜和比铜活泼的金属都失去电子进入溶液,阴极溶液中Cu2+得到电子沉积在阴极上,所以,为阳极a电极连接粗铜,电解一段时间后,溶液中铜离子浓度在减小,
故答案为:粗铜;减小;
(4)生成n(Ag)=$\frac{2.16g}{108g/mol}$=0.02mol,转移电子0.02mol,故答案为:0.02mol.
点评 本题考查了燃料电池和电解池的相关知识,转移电子守恒的应用,题目难度中等.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
11.下列有关物质的分类及判断正确的是( )
| A. | 生石灰、白磷、胆矾、纯碱分别属于氧化物、单质、纯净物、盐 | |
| B. | 按树状分类法,物质可分为纯净物和化合物 | |
| C. | NaCl溶液、KClO3、BaSO4都是电解质 | |
| D. | 按分散质粒子的大小,可以把分散系分为溶液、胶体和浊液,其中胶体和溶液的本质区别在于胶体能发生丁达尔效应 |
12.下列反应符合“电解质+电解质=电解质”的是( )
| A. | NH3+HCl═NH4Cl | B. | H2S+Na2S═2NaHS | ||
| C. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | D. | CO2+NaOH═NaHCO3 |
8.(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2165kJ/mol.又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是1016.5kJ.
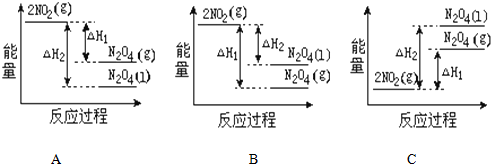
(2)已知:2NO2(g)═N2O4(g)△H1 2NO2(g)═N2O4(l)△H2
下列能量变化示意图中,正确的是(选填字母)A.
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2 599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变(列出简单的计算式):+226.7kJ•mol-1.
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体(结构简式为CH3OH). 已知某些化学键的键能数据如表:
已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1.
(2)已知:2NO2(g)═N2O4(g)△H1 2NO2(g)═N2O4(l)△H2
下列能量变化示意图中,正确的是(选填字母)A.

(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2 599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变(列出简单的计算式):+226.7kJ•mol-1.
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体(结构简式为CH3OH). 已知某些化学键的键能数据如表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
15.实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,回答下列问题:
(1)已知某温度下某反应的化学平衡常数表达式为:K=$\frac{c({H}_{2}O)}{c(CO)•c({H}_{2})}$,所对应的化学反应方程式为:CO(g)+H2(g)?C(s)+H2O(g).
(2)已知在一定温度下,
①C(s)+CO2(g)?2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:K3=K1×K2,△H3=(a+b)kJ/mol(用含a、b的代数式表示).
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示:
该反应的正反应方向是放热反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol•L-1,在该条件下,CO的平衡转化率为:75%.
(4)在催化剂存在条件下反应:H2O(g)+CO(g)?CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图1所示:

对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=$\frac{P(CO{\;}_{2})P(H{\;}_{2})}{P(CO)P(H{\;}_{2}O)}$,提高p[H2O(g)]/p(CO)比,则Kp不变(填“变大”、“变小”或“不变”).实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右、p[H2O(g)]/p(CO)=3~5.其原因可能是投料比太低,CO的转化率不太高,而投料比3~5时转化率已经很高达到96%~98%,再增加投料比,需要大大的增加蒸汽添加量,这样在在经济上不合算,催化剂的活性温度在400℃左右.
(5)工业上可利用原电池原理除去工业尾气中的CO并利用其电能,反应装置如图2所示,请写出负极的电极反应式:CO-2e-+CO32-=2CO2.
(1)已知某温度下某反应的化学平衡常数表达式为:K=$\frac{c({H}_{2}O)}{c(CO)•c({H}_{2})}$,所对应的化学反应方程式为:CO(g)+H2(g)?C(s)+H2O(g).
(2)已知在一定温度下,
①C(s)+CO2(g)?2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:K3=K1×K2,△H3=(a+b)kJ/mol(用含a、b的代数式表示).
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)在催化剂存在条件下反应:H2O(g)+CO(g)?CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图1所示:

对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=$\frac{P(CO{\;}_{2})P(H{\;}_{2})}{P(CO)P(H{\;}_{2}O)}$,提高p[H2O(g)]/p(CO)比,则Kp不变(填“变大”、“变小”或“不变”).实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右、p[H2O(g)]/p(CO)=3~5.其原因可能是投料比太低,CO的转化率不太高,而投料比3~5时转化率已经很高达到96%~98%,再增加投料比,需要大大的增加蒸汽添加量,这样在在经济上不合算,催化剂的活性温度在400℃左右.
(5)工业上可利用原电池原理除去工业尾气中的CO并利用其电能,反应装置如图2所示,请写出负极的电极反应式:CO-2e-+CO32-=2CO2.
5.下列说法正确的是( )
| A. | 能电离出H+的化合物叫做酸 | |
| B. | 实验测得1mol某气体体积为22.4L,测定条件一定是标准状况 | |
| C. | 将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 | |
| D. | 碱性氧化物一定是金属氧化物 |
9.下列有关实验的说法不正确的是( )
| A. | 为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液进行酸化 | |
| B. | 实验室配制FeCl3溶液时,先将FeCl3溶于浓盐酸再加水稀释 | |
| C. | 从海带灰中提取碘时,为了使I-既能完全转化为I2,又对环境无影响,可选H2O2作氧化剂 | |
| D. | 制备硫酸亚铁铵晶体,在蒸发皿中蒸发浓缩溶液时,不能将溶液全部蒸干 |
10.下列变化过程中,△S<0的是( )
| A. | 氯化钠溶于水中 | B. | NH3(g)与HCl(g)反应生成NH4Cl(s) | ||
| C. | 干冰(CO2)的升华 | D. | CaCO3(s)分解为CaO(s)和CO2(g) |
 (1)1.00g CH4完全燃烧生成液态水和CO2,放出55.6kJ热量,写出表示CH4的燃烧热的热化学方程式CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ•mol-1.
(1)1.00g CH4完全燃烧生成液态水和CO2,放出55.6kJ热量,写出表示CH4的燃烧热的热化学方程式CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6KJ•mol-1.