题目内容
(14分)人工固氮是指将氮元素由游离态转化为化合态的过程。
I.最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实验氮的固定一电解法合成氨,大大提高了氮气和氢气的转化率。
总反应式为:N2+3H2  2NH3
2NH3
则在电解法合成氨的过程中,应将H2不断地通入_________极(填“阴”或“阳”) ;
向另一电极通入N2,该电极的反应式为__________________________。
II.据报道,在一定条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,主要产物为NH3相应的反应方程式为:2N2(g)+6 H2O (g)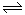 4NH3(g)+3O2(g) △H=Q ①
4NH3(g)+3O2(g) △H=Q ①
(1)上述反应的平衡常数表达式为_______________。
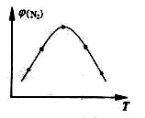
(2)取五份等体积N2和H2O的混合气体(物质的量之比均为1:3), 分别加 入体积相同的恒容密闭容器中,在温度不相同的情况下发生反应,反应相同时间后,测得氮气的体积分数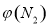 与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
与反应温度T的关系曲线如下图所示,则上述反应的Q________0(填“>”、“<”或“=”)。
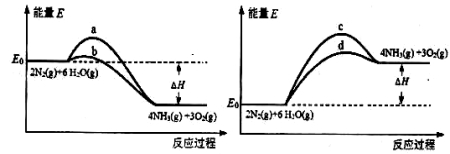
(3)若上述反应在有催化剂的情况下发生,则下图所示的a、b、c、d四条曲线中,能表示反应体系能量变化的是_______(填字母代号),图中△H绝对值为1530kJ·mol-1。
III.目前工业合成氨的原理是: N2(g)+3H2(g)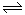 2NH3(g) △H=-93.0kJ/mol ②
2NH3(g) △H=-93.0kJ/mol ②
回答下列问题:
(1)结合II中的数据,则2H2(g)+ O2(g)=2 H2O (g)的△H=___________。
(2)在一定温度下,将1molN2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。
①达平衡时,H2的转化率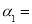 ______________。
______________。
②在相同条件下,若起始时只将NH3置于该容器中,达到平衡状态时NH3的转化率
为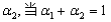 时,则起始时NH3的物质的量
时,则起始时NH3的物质的量 _________mol。
_________mol。
(14分)Ⅰ. 阳(2分) N2+6H++6e-===2NH3 (2分)
Ⅱ.(1)K=c(NH3)4·c(O2)3/c(N2)2·c(H2O)6(2分)
(2)>(1分) (3)d(1分)
Ⅲ. (1)-572.0 kJ·mol-1(2分,单位不写不给分)
(2)①60%(2分) ②2(2分)
【解析】
试题分析:I. 在电解法合成氨的过程中,氢气发生氧化反应,所以通入电解池的阳极,另一极通入氮气,则氮气发生还原反应,与阳极产生的氢离子结合 氨气,电极反应式为N2+6H++6e-===2NH3;
II.(1)根据平衡常数的表达式可知该反应的平衡常数K= c(NH3)4·c(O2)3/c(N2)2·c(H2O)6;
(2)图像的最高点表示反应达到平衡时氮气得体积分数,随温度升高,氮气得体积分数减小,说明升高温度平衡正向移动,所以正向是吸热反应,所以Q>0;
(3)2N2(g)+6 H2O (g)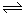 4NH3(g)+3O2(g) △H=Q是吸热反应,则反应物的总能量低于生成物的总能量,且使用催化剂,可以降低反应的活化能,而反应热不变,所以应选择d曲线;
4NH3(g)+3O2(g) △H=Q是吸热反应,则反应物的总能量低于生成物的总能量,且使用催化剂,可以降低反应的活化能,而反应热不变,所以应选择d曲线;
III.(1)由II知Q=+1530kJ/mol,根据盖斯定律得所求方程式2H2(g)+ O2(g)=2 H2O (g)的△H=(②×2-①)/3=[(-93.0)×2-1530]kJ/mol/3=-572.0kJ/mol;
(2)①设反应达平衡时消耗氮气得物质的量是xmol,则
N2(g)+3H2(g)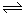 2NH3(g)
2NH3(g)
开始时(mol) 1 3
转化的(mol) x 3x 2x
平衡时(mol) 1-x 3-3x 2x
根据题意有1-x+3-3x+2x=2.8,所以x=0.6mol,则氢气的转化率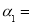 3x/3×100%=60%;
3x/3×100%=60%;
②当α1+α2=1时说明只将NH3置于该容器中,达到平衡状态与原平衡是等效平衡,则将氮气、氢气全部转化为氨气的物质的量即可达到等效平衡,所以1mol氮气、3mol氢气完全转化为氨气的物质的量是2mol.
考点:考查电化学原理的应用,化学平衡理论的应用,平衡常数的表示,反应热效应的判断,盖斯定律的应用,等效平衡的判断,转化率的计算

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案 Mgx Mo3S4 。下列说法错误的是( )
Mgx Mo3S4 。下列说法错误的是( )
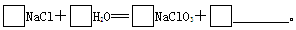

 )和抗癫痫药物H(
)和抗癫痫药物H( )的路线如下(部分反应略去条件和试剂):
)的路线如下(部分反应略去条件和试剂): 

 + H2O(R、R’表示烃基或氢)
+ H2O(R、R’表示烃基或氢) )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。