题目内容
6.能和甲烷发生取代反应的物质有( )| A. | 溴水 | B. | 氧气 | C. | 氯气 | D. | 氯化氢 |
分析 在光照条件下,烷烃能与卤素单质气体发生取代反应,可以燃烧,烷烃性质稳定,与溴水、氯化氢等不反应.
解答 解:A.甲烷和溴水不能发生化学反应,故A错误;
B.甲烷能在氧气中燃烧,不是取代反应,故B错误;
C.光照条件下,甲烷能与氯气发生取代反应,故C正确;
D.甲烷和氯化氢气体不反应,故D错误;
故选C.
点评 本题考查了甲烷的化学性质,比较基础,掌握甲烷的化学性质是解题的关键,注意在光照条件下,甲烷与卤素单质气体发生取代反应,与溴水不反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.为测定碱式碳酸钴[Cox(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究.已知:碱式碳酸钴受热时可分解生成三种氧化物.
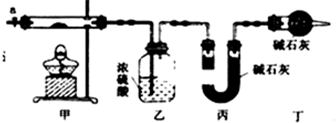
(1)按如图所示装置组装好仪器,并检查装置气密性;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中不再有气泡产生时将装置中(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是生成的CO2和H2O(g)全部排入乙、丙装置.
(2)某同学认为上述实验中存在一个缺陷,该缺陷是未考虑空气中的水蒸气和二氧化碳对实验的影响.
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为Co3(OH)4(CO3)2.
(4)CoCl2•6H2O常用作多彩水泥的添加剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种工艺如下:
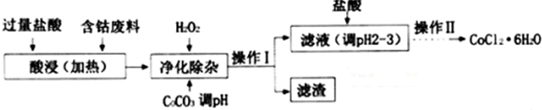
已知:25℃时
①净化除杂时,加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O;
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为Fe(OH)3和Al(OH)3;
③加盐酸调整pH为2~3的目的为抑制CoCl2的水解.

(1)按如图所示装置组装好仪器,并检查装置气密性;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中不再有气泡产生时将装置中(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是生成的CO2和H2O(g)全部排入乙、丙装置.
(2)某同学认为上述实验中存在一个缺陷,该缺陷是未考虑空气中的水蒸气和二氧化碳对实验的影响.
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为Co3(OH)4(CO3)2.
(4)CoCl2•6H2O常用作多彩水泥的添加剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种工艺如下:

已知:25℃时
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀的pH | 4.1 | 9.7 | 9.2 | 5.2 |
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为Fe(OH)3和Al(OH)3;
③加盐酸调整pH为2~3的目的为抑制CoCl2的水解.
17.某化合物有碳、氢、氧三种元素组成,其红外光谱图有C-H键、O-H键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式( )
| A. | CH3CH2OCH3 | B. | CH3CH(OH)CH3 | C. | CH3CH2 CH2CH2OH | D. | CH3CH2CHO |
14.常温下有0.1mol/L的以下几种溶液(①H2SO4溶液、②NaHSO4溶液、③CH3COOH溶液、④HCl溶液、⑤HCN溶液、⑥NH3•H2O),其中如下几种溶液的电离度(即已经电离的占原来总的百分数)如表(已知H2SO4的第一步电离是完全的),回答下面问题:
(1)常温下,pH相同的表格中几种溶液,其物质的量浓度由大到小的顺序是(填序号,下同)③>②>④>①.
(2)常温下,将足量的锌粉投入等体积pH=1的表格中几种溶液中,产生H2的体积(同温同压下)由大到小的顺序是③>②>①>④.
(3)在25℃时,若用已知浓度的NaOH滴定未知浓度的CH3COOH应选用酚酞作指示剂,若终点时溶液pH=a,则由水电离的c(H+)为10(a-14)mol/L.
(4)在25℃时,将bmol•L-1的KCN溶液与0.01mol•L-1的盐酸等体积混合,反应达到平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度b>0.01mol•L-1(填“>”“<”或“=”);用含b的代数式表示HCN的电离常数Ka=(100b-1)×10-7 mol•L-1.
| ①H2SO4溶液中HSO4- | ②NaHSO4溶液中HSO4- | ③CH3COOH | ④HCl溶液 |
| 10% | 29% | 1.33% | 100% |
(2)常温下,将足量的锌粉投入等体积pH=1的表格中几种溶液中,产生H2的体积(同温同压下)由大到小的顺序是③>②>①>④.
(3)在25℃时,若用已知浓度的NaOH滴定未知浓度的CH3COOH应选用酚酞作指示剂,若终点时溶液pH=a,则由水电离的c(H+)为10(a-14)mol/L.
(4)在25℃时,将bmol•L-1的KCN溶液与0.01mol•L-1的盐酸等体积混合,反应达到平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度b>0.01mol•L-1(填“>”“<”或“=”);用含b的代数式表示HCN的电离常数Ka=(100b-1)×10-7 mol•L-1.
11.下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是( )
| A. | CH3Cl | B. | 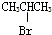 | C. | (CH3)3C-CH2Cl | D. | 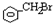 |
18.检验溴乙烷中含有溴元素存在的实验步骤、操作和顺序正确的是( )
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
| A. | ①②④③ | B. | ②④③① | C. | ②④① | D. | ③④① |
 表示的分子式C7H12;名称是3-甲基-2,4-己二烯.
表示的分子式C7H12;名称是3-甲基-2,4-己二烯.