题目内容
10.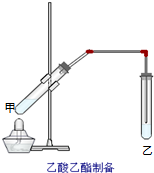 如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:(1)试管乙中观察到的现象是液体分层
(2)试管甲中加入浓硫酸的目的是ac
a.吸水剂 b.脱水剂 c.催化剂 d.氧化剂
(3)该实验中长导管的作用是导气、冷凝其不宜伸入试管乙的溶液中,原因是防止倒吸
(4)试管乙中饱和Na2CO3的作用是除去乙酸乙酯中的乙醇和乙酸,降低乙酸乙酯的溶解度,便于分层
(5)写出试管甲中发生反应的化学方程式CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.
分析 (1)乙酸乙酯与碳酸钠溶液分层,乙酸乙酯的密度比水的密度小;
(2)该反应为可逆反应,且浓硫酸可吸收水;
(3)长导管可导气、冷凝回流,乙酸、乙醇易溶于水,导管口在液面下可发生倒吸;
(4)碳酸钠溶液可吸收乙醇、除去乙酸,降低乙酸乙酯的溶解度;
(5)试管甲中乙酸和乙醇发生酯化反应生成乙酸乙酯和水.
解答 解:(1)乙酸乙酯与碳酸钠溶液分层,乙酸乙酯的密度比水的密度小,则试管乙中观察到的现象是液体分层,
故答案为:液体分层;
(2)该反应为可逆反应,且浓硫酸可吸收水,则浓硫酸的作用为催化剂、吸水剂,故答案为:ac;
(3)该实验中长导管的作用是导气、冷凝,其不宜伸入试管乙的溶液中,原因是防止倒吸,
故答案为:导气、冷凝;防止倒吸;
(4)试管乙中饱和Na2CO3的作用是除去乙酸乙酯中的乙醇和乙酸,降低乙酸乙酯的溶解度,便于分层,
故答案为:除去乙酸乙酯中的乙醇和乙酸,降低乙酸乙酯的溶解度,便于分层;
(5)试管甲中发生反应的化学方程式为CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.
点评 本题考查有机物的制备实验,为高频考点,把握制备实验操作、混合物分离提纯、有机物的性质为解答的关键,侧重分析与实验能力的考查,注意长导管的作用,题目难度不大.

练习册系列答案
相关题目
12.将铝条投到某溶液中产生氢气,则此溶液中一定能够大量共存的离子组是( )
| A. | Ba2+、Cl-、NO3-、K+ | B. | HCO3-、K+、SO42-、Cl- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | Na+、Cl-、K+、SO42-、 |
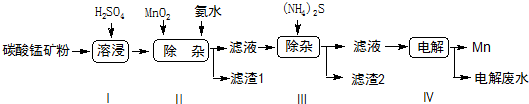
18.锰是冶炼工业中常用的添加剂.以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:
已知25℃,部分物质的溶度积常数如下:
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是MnCO3+H2SO4=MnSO4+CO2↑+H2O.
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,则该反应过程中的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,加氨水调节溶液的pH为5.0-6.0,以除去Fe3+.
(3)步骤Ⅲ中,滤渣2的主要成分是CoS和NiS.
(4)步骤Ⅳ中,在阴(填“阴”或“阳”)极析出Mn,电极反应方程式为Mn2++2e-=Mn.
(5)已知:S(s)+O2(g)=SO2(g)△H=a kJ•mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s)△H=b kJ•mol-1
MnO2(s)+SO2(g)=MnSO4(s)△H=c kJ•mol-1,则Mn的燃烧热△H=-( a+c-b) kJ•mol-1.
(6)按照图示流程,含MnCO3质量分数为57.5%的碳酸锰矿a kg,最终得到Mn的质量为110b kg,忽略中间过程的损耗,则除杂质时,所引入的锰元素相当于MnO2174b-0.435akg.[MnCO3摩尔质量115g/mol,MnO2摩尔质量87g/mol].

已知25℃,部分物质的溶度积常数如下:
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,则该反应过程中的离子方程式是MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,加氨水调节溶液的pH为5.0-6.0,以除去Fe3+.
(3)步骤Ⅲ中,滤渣2的主要成分是CoS和NiS.
(4)步骤Ⅳ中,在阴(填“阴”或“阳”)极析出Mn,电极反应方程式为Mn2++2e-=Mn.
(5)已知:S(s)+O2(g)=SO2(g)△H=a kJ•mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s)△H=b kJ•mol-1
MnO2(s)+SO2(g)=MnSO4(s)△H=c kJ•mol-1,则Mn的燃烧热△H=-( a+c-b) kJ•mol-1.
(6)按照图示流程,含MnCO3质量分数为57.5%的碳酸锰矿a kg,最终得到Mn的质量为110b kg,忽略中间过程的损耗,则除杂质时,所引入的锰元素相当于MnO2174b-0.435akg.[MnCO3摩尔质量115g/mol,MnO2摩尔质量87g/mol].
15. 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
②有关有机物的沸点:
请回答:
(1)浓硫酸的作用是催化剂、吸水剂;
(2)球形干燥管C的作用是防止倒吸反应结束后D中的现象是溶液分层,上层为无色油状液体
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和少量水,应先加入无水氯化钙,分离出乙醇,然后在混合液中加入沸石(或碎瓷片)再加热进行蒸馏,收集77℃左右的馏分,以得一较纯净的乙酸乙酯.
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
(1)浓硫酸的作用是催化剂、吸水剂;
(2)球形干燥管C的作用是防止倒吸反应结束后D中的现象是溶液分层,上层为无色油状液体
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和少量水,应先加入无水氯化钙,分离出乙醇,然后在混合液中加入沸石(或碎瓷片)再加热进行蒸馏,收集77℃左右的馏分,以得一较纯净的乙酸乙酯.
2.用98%、密度为1.84g/cm3的浓H2SO4配制l mol/L的稀硫酸100mL,现给出下列可能用到仪器:
①100mL量筒;
②10mL量筒;
③50mL烧杯;
④托盘天平;
⑤100mL容量瓶;
⑥胶头滴管;
⑦玻璃棒
按使用仪器先后顺序排列正确的是( )
①100mL量筒;
②10mL量筒;
③50mL烧杯;
④托盘天平;
⑤100mL容量瓶;
⑥胶头滴管;
⑦玻璃棒
按使用仪器先后顺序排列正确的是( )
| A. | ②③⑦⑤⑥ | B. | ②⑤⑦⑥ | C. | ①③⑤⑦④⑥ | D. | ④③⑦ |
20.将1mol•L-1NaOH溶液与3mol•L-1NaOH溶液等体积混合,此溶液的物质的量浓度是( )
| A. | 1mol•L-1 | B. | 3mol•L-1 | C. | 2mol•L-1 | D. | 4mol•L-1 |