题目内容
16.如图是自然界中氮循环的一部分,下列有关叙述不正确的是( )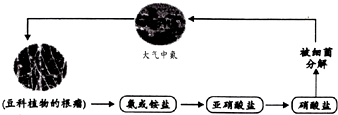
| A. | 在这一循环中氮元素既有被氧化又有被还原 | |
| B. | 其中有一种变化是氮的固定 | |
| C. | 这一循环中氮元素的化合价共有三种 | |
| D. | 由于自然界中氮的循环,使大气中氮气的含量保持稳定 |
分析 A.元素化合价升高,被氧化,元素化合价降低,被还原;
B.氮的固定是将空气中游离态的氮转化为含氮化合物的过程;
C.循环中氮元素的化合价有:-3,0,+3,+5;
D.由于循环,使得氮气的含量保持稳定.
解答 解:A.氮元素的化合价由-3价升高到+3价,氮元素被氧化,氮元素的化合价由+5价降低到0价,氮元素还原,故A正确;
B.大豆的根瘤菌将氮气转变为植物蛋白质,是由氮气转化为氮的化合物,属于氮的固定,故B正确;
C.循环中氮元素的化合价有:-3,0,+3,+5,共4种,故C错误;
D.由于自然界中氮的循环,使大气中氮气的含量保持稳定,故D正确;
故选C.
点评 本题以自然界中氮循环为背景,考查了氧化还原反应、氮的固定,化合价等,属于基础题,难度不大.

练习册系列答案
相关题目
12.下列物质的焰色反应是紫色的是( )
| A. | 钾及其化合物 | B. | 铜及其化合物 | C. | 锂及其化合物 | D. | 钠及其化合物 |
7.已知甲醇的燃烧热数值为726.51kJ•mol-1.下列热化学方程式书写正确的是( )
| A. | CH4O+$\frac{3}{2}$O2═CO2+2H2O△H=-726.51 kJ•mol-1 | |
| B. | CH4O(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H=+726.51 kJ•mol-1 | |
| C. | 2CH4O(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1453.12 kJ•mol-1 | |
| D. | CH4O(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-726.51 kJ•mol-1 |
4.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 0.1 mol Cl2含有的氯原子数为0.1NA | |
| B. | 3.4 g NH3含有的分子数为0.2NA | |
| C. | 标准状况下,22.4 L H2O含有的分子数为NA | |
| D. | 100 mL 0.1 mol/L的Na2SO4溶液中,Na+数为0.01 NA |
11.下列关于钠的说法中不正确的是( )
| A. | 金属钠和氧气反应,条件不同,产物则不同 | |
| B. | 将钠投入氯化铵溶液中会有无色有刺激性气味的气体生成 | |
| C. | 当钠与硫酸铜溶液反应时,有大量红色固体铜生成 | |
| D. | 钠的化学性质比较活泼,少量的钠可以保存煤油中 |
1.配制0.1000mol/LH2SO4溶液250mL,下列有关说法错误的是( )
| A. | 在配制过程中玻璃棒的作用是搅拌和引流 | |
| B. | 用到的仪器有250 mL容量瓶、托盘天平、量筒、烧杯、玻璃棒和胶头滴管 | |
| C. | 浓硫酸在烧杯中稀释后,立即转移到容量瓶进行后续操作,所配溶液浓度偏高 | |
| D. | 液面离容量瓶刻度线1~2cm时,应改用胶头滴管滴加水 |
8.下列关于粒子结构的描述不正确的是( )
| A. | H2S和NH3均是价电子总数为8的极性分子 | |
| B. | OH-和HF均是含有极性键的10电子粒子 | |
| C. | CHCl3和CCl4均是四面体构型的非极性分子 | |
| D. | 1 mol D216O(重水)中含中子、质子、电子各10NA(NA代表阿伏加德罗常数的值) |
5.下列物质不属于强电解质的是( )
| A. | 硫酸 | B. | 醋酸 | C. | 氢氧化钡 | D. | 硫酸钡 |
6.下列说法正确的是( )
| A. | FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 | |
| B. | 食盐水中Ca2+、SO42-等杂质的去除,应先加Na2CO3溶液,后加BaCl2溶液 | |
| C. | 用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 | |
| D. | 用BaCl2溶液来检验暴露在空气中的Na2SO3样品是否变质 |